��Ŀ����
4����������������ѧ�о��IJ�ʢʱ�ڣ���ѧ���о����֣������������ڵ������ӣ��ɽ���1������ת��Ϊ�������������ɻ���O2-����������������һϵ�����ɻ���һ������������������ھ���һ�������Ļ�����ϵͳ��������ø�Ϳ������������ܽ�������ת��Ϊ���Խϵ͵����ʣ���������ܵ����������������ǰ���NH2OH�������ķ������Լ��������ϵͳ��O2-������ԭ����O2-���ǰ���Ӧ����NO2-��һ�ֹ������NO2-�ڶ���������ͦ�-���������£����ɷۺ��ż��Ⱦ�ϣ���Ⱦ���ڦ�=530nm�����������գ���������ֵ��c��NO2-�������ȣ��Ӷ��ɼ������Ʒ�е�O2-������ijʵ���������Ϸ�������������Һ��c��NO2-��=2.500��10-3 mol?L-1����1���뽫�ⶨԭ���йص����ӷ���ʽȱ�ٵ����ʲ�����������ƽ��
1NH2OH+2O2-+1H+=1NO2-+1H2O2+1H2O��
��2���������Ʒ��c��O2-��=5.000��10-3mol•L-1��
��3�������ǰ��������ⶨO2-ʱ���������ɵĹ���������Ϊ������ѡ�����Ե�K2Cr2O7���ж�����������д����Ӧ�����ӷ���ʽCr2O72-+3H2O2+8H+=2Cr3++3O2��+7H2O��
��4��NO-2���������ԣ����л�ԭ�ԣ�NaNO2��������ѪҺʱ���ܽ�Ѫ�쵰���е�Fe2+������Fe3+��������Ѫ�쵰��ת��Ϊ����Ѫ�쵰�ף�ʧȥЯ�����ܣ������ж����������������и����Լ����ܼ���NO2-����C
A��FeCl2 KSCN B��KMnO4 H2SO4
C��AgNO3 HNO3D��KI����
��5��ij�о���ѧϰС�飬Ϊ�о��⻯ѧ�����������ɣ���һ����ʵ�����У������������Ҫ�ɷ�ΪRH��������NO��NO2��O3��PAN��CH3COOONO2�����������ʵ����Ũ����ʱ�����ʧ����¼����ͼ������ͼ�����ݣ��������ۣ����������D
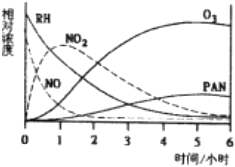
A��NO����ʧ�����ʱ�RH��
B��NO����NO2
C��RH��NO2��������PAN��O3
D��O3����PAN��
���� ��1������������Ϣ��������غ㶨����д��ѧ����ʽ��
��2���������ӷ���ʽ��c��O2-����c��N02-���ļ�������ϵ���㣬c��NH2OH����c��O2-��=1��2��
��3���������Ե�K2Cr2O7���������Ժ�H2O2�Ļ�ԭ�Խ�������غ㶨�ɺ͵���غ���д���ӷ���ʽ��
��4��NO2-���������ԣ����л�ԭ�ԣ��ܽ�Fe2+������Fe3+��������������ѡ���Լ���
��5��A����������������������Ũ�ȣ�
B������ͼ��仯�����ƣ�RH��NO��Ũ��һֱ�ڼ��٣�O3��PAN��Ũ��һֱ�����ӣ�NO2��Ũ�����������٣�
C����ijһʱ����ڵı仯������仯�IJ�ͬ����Ҳ�DZ�����״��㣬��NO��ʧ��������0-1ʱ����ڱ�PH�Ŀ죬��0-1ʱ�����NO��������NO2�ȣ�
D��O3��Ũ��һֱ�ڼ��ٲ������Ƿ�Ӧ�
��� �⣺��1��O2-���ǰ���NH2OH���������Ի����з�Ӧ��NO2-��һ�ֹ���������������غ�ӦΪH2O2��NH2OH+2O2-+H+=NO2-+H2O2+H2O��
�ʴ�Ϊ��1��2��1��1��1H2O2��1��
��2�����ݷ�Ӧʽ��NH2OH+2O2-+H+=NO2-+H2O2+H2O��c��NH2OH����c��O2-��=1��2����c��O2-��=2��2.500��1O-3mol/L=5.000��10-3mol/L��
�ʴ�Ϊ��5.000��10-3mol/L��
��3��Cr2O7���������ԣ�H2O2���л�ԭ�ԣ����߷���������ԭ��Ӧ����Cr3+��O2����Ӧ�����ӷ���ʽΪ��Cr2O72-+3H2O2+8H+=2Cr3++3O2��+7H2O��
�ʴ�Ϊ��Cr2O72-+3H2O2+8H+=2Cr3++3O2��+7H2O��
��4��NO2-���������ԣ����л�ԭ�ԣ��ܽ�Fe2+������Fe3+��
A������FeCl2��KSCNʱ��NO2-��Fe2+������Fe3+��������Һ���ɫ����������FeCl2��KSCN����NO2-����A��ȷ��
B��NO2-�л�ԭ����ʹ���Ը��������Һ��ɫ����������KMnO4��H2SO4����NO2-����B��ȷ��
C���ں���NO2-��Һ�м���AgNO3��HNO3�������������Բ��ܼ��飬��C����
D��NO2-���������ܰѵ���������Ϊ�ⵥ�ʣ�ʹ�⻯�ص�����Һ����ɫ����������KI�͵��ۼ���NO2-����D��ȷ��
�ʴ�Ϊ��C��
��5��A��������б�ʿ�֪��ijһʱ�����NO��ʧ�����ʱ�RH�죬��A��ȷ��
B��NO��Ũ��һֱ�ڼ��٣�NO2��Ũ�������Ӻ���٣���0-1ʱ�����NO��������NO2����B��ȷ��
C��ͼ��O3��PAN��Ũ�����ӣ�RH��Ũ�ȼ��٣�RH��NO2��ijһʱ����ڿ��ܷ�Ӧ����PAN��O3����C��ȷ
D��O3��Ũ��һֱ�����ӣ���������Ϊ��Ӧ���D����
��ѡD��
�ʴ�Ϊ��D��
���� �����Ϊ�ۺϣ��������ε����ʣ���Ҫ������ѧ����������Ϣ�ķ�������������������Ϣ��Ŀ����ʽ���֣��������ʵ���ɺͺ����IJⶨ��ע��������ԭ����ʽ����д����Ŀ�Ѷ��еȣ�

 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�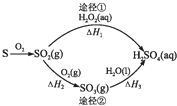
| A�� | ��֪S��l��+O2��g���TSO2��g����H=-293.23kJ•mol-1����S��s��+O2��g���TSO2��g����Ӧ�ų�������С��293.23 kJ/mol | |
| B�� | ��1 mol H2SO4��Ũ��Һ������NaOH��Ӧ���ų���������Ϊ�к��� | |
| C�� | ;������SO2��SO3���������������� | |
| D�� | ����H1����H2+��H3����2H2O2��aq���T2H2O��l��+O2��g��Ϊ���ȷ�Ӧ |
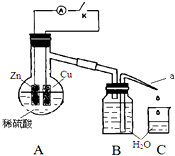 ijͬѧ����Zn��ϡH2SO4�ķ�Ӧ��
ijͬѧ����Zn��ϡH2SO4�ķ�Ӧ����1���÷�Ӧ�����ӷ���ʽ��Zn+2H+=Zn2++H2����
��2����H2ʱ����ϡ���������Ũ���ᣬԭ����ŨH2SO4����ǿ�����ԣ���������������
��3����֪��Zn��s��+$\frac{1}{2}$O2��g��=ZnO��s����H=-332kJ/mol
ZnO��s��+H2SO4��aq��=ZnSO4��aq��+H2O��l����H=-112kJ/mol
H2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-286kJ/mol
��Zn��ϡH2SO4��Ӧ����1mol H2 ʱ�ķ�Ӧ�ȡ�H=-158kJ/mol��
��4����ͬѧ����ͼװ�ý���ʵ�飬����Ӱ�췴Ӧ���ʵ����أ�
ʵ��ʱ���ӶϿ�K��ʼ��ÿ���1���ӣ�����Ͽ���պ�K������������ÿ1 �����ڴ�a��������ˮ�������õ���ˮ�������±���ʾ��
| 1����ˮ�������Ͽ�K�� | 34 | 59 | 86 | 117 | �� | 102 |
| 1����ˮ�������պ�K�� | 58 | 81 | 112 | 139 | �� | 78 |
����ˮ����58��34��81��59��˵���ڷ�Ӧ���ڣ��պ�Kʱ�ȶϿ�Kʱ�ķ�Ӧ���ʿ죨��족������������Ҫԭ�����γ�ԭ��ط�Ӧ�ٶȿ죮
����ˮ����102��78��˵���ڷ�Ӧ���ڣ��Ͽ�Kʱ�ķ�Ӧ���ʿ��ڱպ�Kʱ�ķ�Ӧ���ʣ���Ҫԭ������Һ�е�c��H+�����ڱպ�Kʱ��Һ�е�c��H+����
�۴�����ת����ʽ��ͬ�ĽǶȣ�����ˮ����86��81��117��112����Ҫԭ���ǶϿ�Kʱ����Ӧ�Ļ�ѧ����Ҫת�������ܣ��պ�Kʱ����Ӧ�Ļ�ѧ����Ҫת���ɵ��ܣ�ǰ��ʹ��Һ���¶����ø��ߣ��ʷ�Ӧ���ʸ��죮
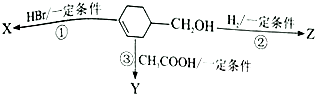 ���
�л��� 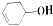 �ɷ�������ͼʾ��Ӧ����֪����Y����֬�࣮����˵����ȷ���ǣ�������
�ɷ�������ͼʾ��Ӧ����֪����Y����֬�࣮����˵����ȷ���ǣ�������| A�� | ��Ӧ�۵�������ϡ���ᡢ���� | B�� | ��Ӧ�٢ڵ����Ͳ�������ͬ | ||
| C�� | �л�����X��һ�ִ����� | D�� | Y��Z����ʹ���Ը��������Һ��ɫ |
| A�� | ��ȥNaCl����������KNO3�����Խ�������Ƴ��ȵı�����Һ��Ȼ����ȴ�ᾧ�����ˣ�ϴ�ӣ����� | |
| B�� | ��ʳ�����Ậ���ⶨʵ���У�����NaOH����Һ����Ҫ���ڱ���������ضԸ���ҺŨ�Ƚ��б궨 | |
| C�� | ����ֲ����и��������������˴Ӻ���Ʒ����ȡ���ǹ�ҵ�ϻ�ȡ�����Ҫ;������ҵ�Ӻ�������ȡ�⾭���IJ����У�����-����-����-��ȡ-�ֵ��ᴿ | |
| D�� | �ڽྻ�Թ��м���2mL 10% NaOH��Һ���ټ��������CuSO4��Һ���Ƶõ�����������ͭ����Һ�����ڼ�����������Һ�������Ǻ����Ƿ�ƫ�� |
| A�� | �������ϩ | B�� | ����ͱ�ϩ | C�� | �������ϩ | D�� | ����ͱ�ϩ |
| A�� | NH3��0.002 mol•L-1•s-1 | B�� | H2O��0.0015 mol•L-1•s-1 | ||
| C�� | NO��0.0015 mol•L-1•s-1 | D�� | O2��0.00125 mol•L-1•s-1 |
| A�� | пƬ�ܽ���1mol��ͭƬ������1mol���� | |
| B�� | пƬ������ԭ��Ӧ | |
| C�� | ����������SO42-����Ũ�������� | |
| D�� | ��ع���ʱ������������ͨ�����·���� |
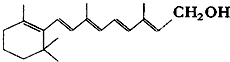 ��֪ά����A1�ļ���ʽ���£��ߵĽ�����˵㴦����̼ԭ�ӣ�������ԭ�Ӳ����ļۣ���C��Hԭ��δ��dz�����
��֪ά����A1�ļ���ʽ���£��ߵĽ�����˵㴦����̼ԭ�ӣ�������ԭ�Ӳ����ļۣ���C��Hԭ��δ��dz�����