题目内容
19.下列化合物的结构中,只含有离子键的是( )| A. | H2O | B. | NaCl | C. | NaOH | D. | CO2 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,以此来解答.
解答 解:A.水中只含共价键,故A不选;
B.氯化钠只含离子键,故B选;
C.NaOH含离子键和O-H共价键,故C不选;
D.二氧化碳只含共价键,故D不选;
故选B.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
相关题目
9.一种气态烷烃和气态烯烃组成的混合物共10g,混合气体密度是相同状况下H2密度的12.5倍,该混合气体通过装有溴水的试剂瓶时,试剂瓶总质量增加了8.4g,组成该混合气体的成分可能是( )
| A. | 乙烷和乙烯 | B. | 甲烷和丙烯 | C. | 甲烷和乙烯 | D. | 丙烷和丙烯 |
10.下列关于价电子构型3s23p4的描述正确的是( )
| A. | 它的元素符号为O | |
| B. | 它的核外电子排布式为1s22s22p63s23p4 | |
| C. | 它的氢化物的电子式为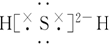 | |
| D. | 其电子排布图为 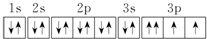 |
7.我国科学家首次合成了一种过渡金属的新核素${\;}_{72}^{185}$Hf,其单质有延展性、不易被腐蚀等特点,可应用于高科技领域.185Hf可由180Hf转化而成,下列有关180Hf、185Hf说法正确的是( )
| A. | 180Hf转化为185Hf是化学变化 | |
| B. | 二者的核外电子数分别为108、113 | |
| C. | 1mol 180Hf的中子数比1mol 185Hf少5NA | |
| D. | 在元素周期表中的位置不同 |
14.以锌片和铜片为电极,以稀硫酸为电解质溶液的原电池中,当导线中通过2mol电子时,下列说法正确的是( )
| A. | 锌片溶解了1mol,铜片上析出1mol氢气 | |
| B. | 锌片发生还原反应 | |
| C. | 正极附近的SO42-离子浓度逐渐增大 | |
| D. | 电池工作时,电子由正极通过外电路流向负极 |
4.根据表中信息判断,下列选项不正确的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4- | Cl2、Mn2+ |
| A. | 第①组反应的其余产物为H2O和 O2 | |
| B. | 第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2 | |
| C. | 第③组反应中生成1 mol Cl2,转移电子2 mol | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |
11.溶液的pH、体积相同的盐酸和醋酸两种溶液,下列叙述错误的是( )
| A. | 它们与NaOH完全中和时,醋酸溶液所消耗的NaOH少 | |
| B. | 它们分别与足量CaCO3反应时,放出的CO2一样多 | |
| C. | 两种溶液的n(Cl-)=n(CH3COO-)相同 | |
| D. | 分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-) |
8.根据有机化合物的命名原则,下列命名正确的是( )
| A. |  3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | |
| B. | 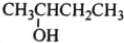 2-羟基丁烷 2-羟基丁烷 | |
| C. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | |
| D. | CH3CH(CH3)CH2COOH 3-甲基丁酸 |
9.下列实验操作中正确的是( )
| A. | 蒸馏实验中,温度计水银球应位于蒸馏烧瓶中液面以下 | |
| B. | 制备乙酸乙酯的实验中,导管末端要伸入饱和Na2CO3溶液液面下 | |
| C. | 分液操作中,待下层液体流出后,将上层液体从分液漏斗上口倒出 | |
| D. | 测定溶液pH时,可用pH试纸蘸取少量待测液并与标准比色卡比较 |