题目内容
13.下列离子方程式的书写,正确的是( )| A. | 足量的烧碱溶液与二氧化碳的反应:OH-+CO2═HCO3- | |
| B. | 盐酸溶液与硝酸银溶液反应:HCl+Ag+═AgCl↓+H+ | |
| C. | 向Na2SiO3溶液中通入少量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| D. | 将稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
分析 A.烧碱过量,反应生成碳酸钠和水;
B.氯化氢为强电解质,应拆成离子形式;
C.二氧化碳少量反应生成硅酸沉淀和碳酸钠;
D.不符合反应客观事实.
解答 解:A.足量的烧碱溶液与二氧化碳的反应,离子方程式:2OH-+CO2═H2O+CO32-,故A错误;
B.盐酸溶液与硝酸银溶液反应,离子方程式:Cl-+Ag+═AgCl↓,故B错误;
C.向Na2SiO3溶液中通入少量CO2,离子方程式:SiO32-+CO2+H2O═H2SiO3↓+CO32-,故C正确;
D.铜与稀硫酸不反应,故D错误;
故选:C.
点评 本题考查了离子方程式正误判断,明确反应实质及离子方程式书写方法是解题关键,注意离子反应遵循客观事实,题目难度中等.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
3.某化学小组同学用下列装置(气密性已检验)进行实验.
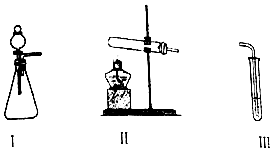
探究O2与KI溶液发生反应的条件.
①甲、乙同学选用以下试剂进行实验(0.1mol•L-1KI溶液,30%H2O2溶液、0.1mol•L-1H2SO4溶液、淀粉溶液、MnO2固体、KMnO4固体),实验记录如表.
甲制取O2的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
乙实验中O2与KI溶液反应的离子方程式是O2+4I-+4H+=2I2+2H2O.
②甲用II加入试剂替换I后,III中仍加入KI、淀粉溶液,再次实验时III中溶液不变蓝.由此他猜测第一次实验时可能是I中的白雾使溶液变蓝.甲又将I中产生的气体直接通入下列a溶液(填序号),证明了白雾中含有H2O2.
a.酸性KMnO4 b.FeCl2 c.Na2S
③由甲、乙两同学的实验,可得出结论:KI溶液在酸性条件下易被O2氧化.

探究O2与KI溶液发生反应的条件.
①甲、乙同学选用以下试剂进行实验(0.1mol•L-1KI溶液,30%H2O2溶液、0.1mol•L-1H2SO4溶液、淀粉溶液、MnO2固体、KMnO4固体),实验记录如表.
| 操作 | 现象 | |
| 甲 | 向I中加入必要的试剂,并向III中加入KI、淀粉溶液.连接I、III,打开活塞 | I中剧烈反应,产生无色气体并伴随大量白雾;III中有气泡冒出,溶液迅速变蓝 |
| 乙 | 向II中加入必要的试剂,并向III中加入KI、淀粉溶液和稀硫酸.连接II、III,点燃酒精灯 | III中有气泡冒出,溶液变蓝 |
乙实验中O2与KI溶液反应的离子方程式是O2+4I-+4H+=2I2+2H2O.
②甲用II加入试剂替换I后,III中仍加入KI、淀粉溶液,再次实验时III中溶液不变蓝.由此他猜测第一次实验时可能是I中的白雾使溶液变蓝.甲又将I中产生的气体直接通入下列a溶液(填序号),证明了白雾中含有H2O2.
a.酸性KMnO4 b.FeCl2 c.Na2S
③由甲、乙两同学的实验,可得出结论:KI溶液在酸性条件下易被O2氧化.
18.下列各组中的两种有机物,其最简式相同但不是同系物的是( )
| A. | 甲酸与硬脂酸 | B. | 甲醇与甘油 | C. | 苯酚与苯甲醇 | D. | 苯与苯乙烯 |
5.下列化学用语表示正确的是( )
| A. | 乙炔的结构简式:CHCH | B. | OH-的电子式: | ||
| C. | F-的结构示意图: | D. | CCl4的比例模型: |
2.等体积硫酸铝、硫酸锌、硫酸钠溶液分别跟足量氯化钡溶液反应,若生成的硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐溶液的物质的量浓度之比为( )
| A. | 1:2:3 | B. | 1:6:9 | C. | 1:3:4 | D. | 1:3:6 |