题目内容
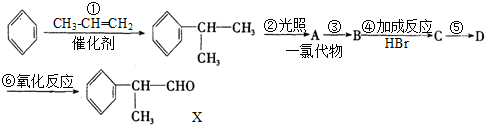
化合物Ⅲ具有水果香味,在实验室可通过如下反应制得:

化合物I可通过下列路径合成:

(1)化合物Ⅱ能使Br2的CCl4溶液褪色,其反应化学方程式为 .
(2)化合物Ⅳ的结构简式为 ,生成化合物Ⅳ的反应类型为 .
(3)在浓硫酸和加热条件下,化合物I易发生消去反应生成含2个甲基的产物,该反应化学方程式为 .
(4)写出满足下列条件的化合物Ⅱ的三种同分异构体 、 、 .
①含一个六元环 ②无酸性,酸性条件下水解生成两种有机物 ③能发生银镜反应
(5)CH3CH2MgBr和 也能发生类似V→Ⅵ的反应,请写出所生成醇的结构简式 .
也能发生类似V→Ⅵ的反应,请写出所生成醇的结构简式 .

化合物I可通过下列路径合成:

(1)化合物Ⅱ能使Br2的CCl4溶液褪色,其反应化学方程式为
(2)化合物Ⅳ的结构简式为
(3)在浓硫酸和加热条件下,化合物I易发生消去反应生成含2个甲基的产物,该反应化学方程式为
(4)写出满足下列条件的化合物Ⅱ的三种同分异构体
①含一个六元环 ②无酸性,酸性条件下水解生成两种有机物 ③能发生银镜反应
(5)CH3CH2MgBr和
 也能发生类似V→Ⅵ的反应,请写出所生成醇的结构简式
也能发生类似V→Ⅵ的反应,请写出所生成醇的结构简式考点:有机物的合成
专题:有机物的化学性质及推断
分析:(1)物质Ⅱ含有碳碳双键,与溴发生加成反应;
(2)对比甲苯与物质V的结构可以判断Ⅳ的结构简式为 ,则甲苯中甲基上的H原子被氯原子取代生成Ⅳ;
,则甲苯中甲基上的H原子被氯原子取代生成Ⅳ;
(3)在浓硫酸和加热条件下,化合物I易发生消去反应生成含2个甲基的产物,发生醇的消去反应生成 与水;
与水;
(4)化合物Ⅱ的不饱和度为3,其同分异构体满足:②无酸性,酸性条件下水解生成两种有机物,含有酯基,③能发生银镜反应,应是甲酸形成的酯基,①含一个六元环,则六元环中含有碳碳双键,固定碳碳双键位置,移动-OOCH书写同分异构体的结构简式;
(5)CH3CH2MgBr和 也能发生类似V→Ⅵ的反应,先发生类似加成反应得到中间产物,CH3CH2-连接醛基中的碳原子、-MgBr连接醛基中的O原子,然后发生水解反应,-OMgBr转化为-OH.
也能发生类似V→Ⅵ的反应,先发生类似加成反应得到中间产物,CH3CH2-连接醛基中的碳原子、-MgBr连接醛基中的O原子,然后发生水解反应,-OMgBr转化为-OH.
(2)对比甲苯与物质V的结构可以判断Ⅳ的结构简式为
 ,则甲苯中甲基上的H原子被氯原子取代生成Ⅳ;
,则甲苯中甲基上的H原子被氯原子取代生成Ⅳ;(3)在浓硫酸和加热条件下,化合物I易发生消去反应生成含2个甲基的产物,发生醇的消去反应生成
 与水;
与水;(4)化合物Ⅱ的不饱和度为3,其同分异构体满足:②无酸性,酸性条件下水解生成两种有机物,含有酯基,③能发生银镜反应,应是甲酸形成的酯基,①含一个六元环,则六元环中含有碳碳双键,固定碳碳双键位置,移动-OOCH书写同分异构体的结构简式;
(5)CH3CH2MgBr和
 也能发生类似V→Ⅵ的反应,先发生类似加成反应得到中间产物,CH3CH2-连接醛基中的碳原子、-MgBr连接醛基中的O原子,然后发生水解反应,-OMgBr转化为-OH.
也能发生类似V→Ⅵ的反应,先发生类似加成反应得到中间产物,CH3CH2-连接醛基中的碳原子、-MgBr连接醛基中的O原子,然后发生水解反应,-OMgBr转化为-OH.解答:
解:(1)物质Ⅱ含有碳碳双键,与溴发生加成反应,该反应方程式为 ,
,
故答案为: ;
;
(2)对比甲苯与物质V的结构可以判断Ⅳ的结构简式为 ,则甲苯中甲基上的H原子被氯原子取代生成Ⅳ,所以反应类型为取代反应,
,则甲苯中甲基上的H原子被氯原子取代生成Ⅳ,所以反应类型为取代反应,
故答案为: ;取代反应;
;取代反应;
(3)在浓硫酸和加热条件下,化合物I易发生消去反应生成含2个甲基的产物,发生醇的消去反应生成 与水,则反应方程式为
与水,则反应方程式为 ,故答案为:
,故答案为: ;
;
(4)化合物Ⅱ的不饱和度为3,其同分异构体满足:②无酸性,酸性条件下水解生成两种有机物,含有酯基,③能发生银镜反应,应是甲酸形成的酯基,①含一个六元环,则六元环中含有碳碳双键,固定碳碳双键位置,移动-OOCH书写同分异构体的结构简式,则符合条件的结构简式为 、
、 、
、 ,故答案为:
,故答案为: ;
; ;
; ;
;
(5)CH3CH2MgBr和 也能发生类似V→Ⅵ的反应,先发生类似加成反应得到中间产物,CH3CH2-连接醛基中的碳原子、-MgBr连接醛基中的O原子,然后发生水解反应,-OMgBr转化为-OH,则生成醇的结构简式为
也能发生类似V→Ⅵ的反应,先发生类似加成反应得到中间产物,CH3CH2-连接醛基中的碳原子、-MgBr连接醛基中的O原子,然后发生水解反应,-OMgBr转化为-OH,则生成醇的结构简式为 ,故答案为:
,故答案为: .
.
 ,
,故答案为:
 ;
;(2)对比甲苯与物质V的结构可以判断Ⅳ的结构简式为
 ,则甲苯中甲基上的H原子被氯原子取代生成Ⅳ,所以反应类型为取代反应,
,则甲苯中甲基上的H原子被氯原子取代生成Ⅳ,所以反应类型为取代反应,故答案为:
 ;取代反应;
;取代反应;(3)在浓硫酸和加热条件下,化合物I易发生消去反应生成含2个甲基的产物,发生醇的消去反应生成
 与水,则反应方程式为
与水,则反应方程式为 ,故答案为:
,故答案为: ;
;(4)化合物Ⅱ的不饱和度为3,其同分异构体满足:②无酸性,酸性条件下水解生成两种有机物,含有酯基,③能发生银镜反应,应是甲酸形成的酯基,①含一个六元环,则六元环中含有碳碳双键,固定碳碳双键位置,移动-OOCH书写同分异构体的结构简式,则符合条件的结构简式为
 、
、 、
、 ,故答案为:
,故答案为: ;
; ;
; ;
;(5)CH3CH2MgBr和
 也能发生类似V→Ⅵ的反应,先发生类似加成反应得到中间产物,CH3CH2-连接醛基中的碳原子、-MgBr连接醛基中的O原子,然后发生水解反应,-OMgBr转化为-OH,则生成醇的结构简式为
也能发生类似V→Ⅵ的反应,先发生类似加成反应得到中间产物,CH3CH2-连接醛基中的碳原子、-MgBr连接醛基中的O原子,然后发生水解反应,-OMgBr转化为-OH,则生成醇的结构简式为 ,故答案为:
,故答案为: .
.
点评:本题考查有机物合成,侧重考查分析、推断、综合应用能力,明确物质中官能团及其性质的关系是解本题关键,注意反应前后物质分子结构的变化,知道其断键和成键方式,难点是自己设计合成路线,要求学生对有机反应类型、反应条件、官能团熟练掌握并灵活应用,题目难点中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
把铜片和锌片放在盛有稀硫酸的表面皿(Ⅰ)中.把石墨a和石墨b放在盛有饱和食盐水的表面皿(Ⅱ)中.如下图所示.下列说法不正确的是( )


| A、表面皿Ⅰ和表面皿Ⅱ中溶液pH不断升高 |
| B、锌片和石墨a均发生氧化反应.铜片和石墨a上均有H2放出 |
| C、表面皿Ⅰ溶液中c(Zn2+)浓度增大 |
| D、石墨b附近滴加酚酞变红 |
用已知浓度的NaOH溶液滴定未知浓度的盐酸溶液,下列说法正确的是会使测定结果偏高的( )
| A、滴定前对碱式滴定管仰视读数,滴定后又俯视,会使测定结果偏高 |
| B、滴定管和锥形瓶使用之前均需用所装溶液润洗 |
| C、用酚酞做指示剂,滴定终点是当最后一滴NaOH溶液滴入时,溶液颜色由无色变为浅红色,且半分钟内不变色 |
| D、滴定前锥形瓶内含有少量水对实验结果无影响 |
某种一元强碱MOH溶液加入一种一元酸HA反应后,溶液呈中性,下列判断一定正确的是( )
| A、加入的酸过量 |
| B、生成的盐不水解 |
| C、酸和碱等物质的量混合 |
| D、反应后溶液中c(A-)=c(M+) |
已知①当溶液中某种离子浓度小于10-5mol/L时即可看作完全沉淀; ②常温下Cu(OH)2的Ksp=2.2×10-20,Fe(OH)3的Ksp=1.25×10-36; ③lg2=0.3.
现有浓度均为0.022mol/L的CuSO4、Fe2(SO4)3的混合溶液,下列说法正确的是( )
现有浓度均为0.022mol/L的CuSO4、Fe2(SO4)3的混合溶液,下列说法正确的是( )
| A、当调节溶液的pH至3.7时,Fe3+才能完全沉淀 |
| B、当c(OH-)达到10-9时,Cu2+开始沉淀,此时Fe3+尚未沉淀完全 |
| C、原溶液中,c(SO42-):[c(Cu2+)+c(Fe3+)]=4:3 |
| D、若要除去上述混合溶液中的Fe3+,加入NaOH固体比加入Cu(OH)2效果好 |
下列各组中的离子,能在溶液中大量共存的是( )
| A、Na+、Cu2+、Cl-、SO42- |
| B、Na+、H+、NO3-、CO32- |
| C、Na+、H+、OH-、SO42- |
| D、Ba2+、Cu2+、Cl-、SO42- |

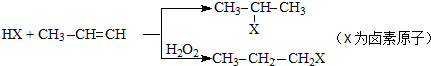
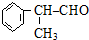 ,该物质是一种香料.
,该物质是一种香料.