题目内容
13.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示.已知Y和W的原子序数之和是Z的3倍,下列说法正确的是( )| Y | Z | ||
| X | W |
| A. | 原子半径:X>Z>W | |
| B. | 气态氢化物的稳定性:Y>Z>W | |
| C. | Z、W均可形成含Y元素的离子化合物 | |
| D. | 最高价氧化物对应水化物的酸性:Y>X>W |
分析 Y、W的原子序数之和是Z的3倍,设Y的原子序数为x,则Z的原子序数为x+1,W的原子序数为x+10,则x+x+10=3×(x+1),解得x=7,即Y为N,结合位置关系可知,Z为O,X为Si,W为Cl,然后结合元素化合物知识来解答.
解答 解:Y、W的原子序数之和是Z的3倍,设Y的原子序数为x,则Z的原子序数为x+1,W的原子序数为x+10,则x+x+10=3×(x+1),解得x=7,即Y为N,结合位置关系可知,Z为O,X为Si,W为Cl.
A.同周期自左而右原子半径减小,电子层越多原子半径越大,则原子半径为X>W>Z,故A错误;
B.非金属性越强,气态氢化物越稳定,则气态氢化物的稳定性为Y<Z,故B错误;
C.Z、W均可形成含有N元素的离子化合物,如NH4NO3、NH4Cl,故C正确;
D.Cl的最高价氧化物对应水化物的酸性为含氧酸中酸性最强的酸,非金属性越强最高价含氧酸的酸性越强,故最高价氧化物对应水化物的酸性:W>Y>X,故D错误,
故选C.
点评 本题可知位置、结构与性质关系,熟练掌握周期表的计算,根据原子序数的关系推断元素为解答的关键,注意对元素周期律的理解应用,题目难度不大.

练习册系列答案
相关题目
1.铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列判断正确的是( )


| A. | K闭合时,c电极反应式:PbSO4+2H2O-2e-=PbO2+4H++SO42- | |
| B. | 当电路中转移0.4mol电子时,I中消耗的H2SO4为0.2 mol | |
| C. | K闭合时,II中SO42-向c电极迁移 | |
| D. | K闭合一段时间后,II可单独作为电源,d电极为正极 |
5.下列实验操作、实验现象和结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向AgNO3溶液中加入过量氨水 | 由白色沉淀生成 | Ag+与NH3•H2O不能共存 |
| B | 向2ml2%的CuSO4溶液中加入0.5mol/L的NaOH溶液,震荡后低价几滴M溶液,加热 | 未出现砖红的沉淀 | M不属于醛类物质 |
| C | 向NaAlO2溶液中滴加饱和NaHCO3溶液 | 由白色沉淀生成 | 验证两者都发生了水解反应,且相互促进 |
| D | 向草酸溶液中低价几滴紫色酸性KmnO4溶液,震荡 | 溶液紫色褪去 | 草酸具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
14.下列实验操作或方法中,不合理的是( )
| A. | 用钥匙取用少量二氧化锰粉末 | |
| B. | 向燃着的酒精灯中直接添加酒精 | |
| C. | 实验室加热高猛酸钾制氧气的装置制取氨气 | |
| D. | 实验室将少量金属钠保存在煤油中 |
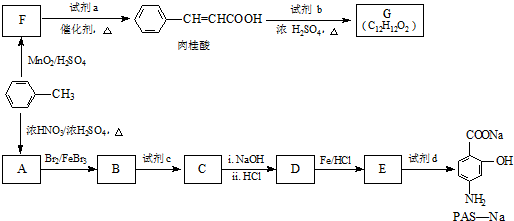
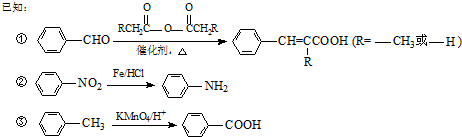
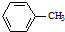 生成A的反应类型是取代反应.
生成A的反应类型是取代反应.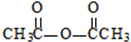 .
.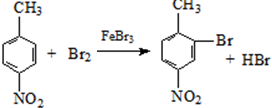 .
.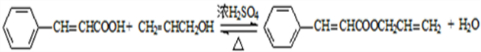 .
. .
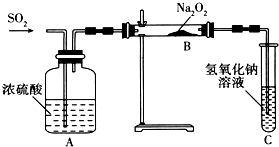
.
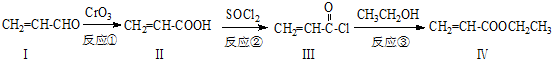
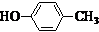 也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为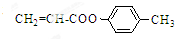 .
.