题目内容
下列说法正确的是( )
| A、只有在原子中,质子数才与核外电子数相等 |
| B、O2-半径比F-的小 |
| C、Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 |
| D、P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的弱 |
考点:质量数与质子数、中子数之间的相互关系,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.原子不带电,分子也不带电,则质子数等于核外电子数;
B.电子排布相同的离子,原子序数越大,半径越小;
C.同主族从上到下金属性增强,失电子能力增强;
D.同主族从上到下非金属性减弱,对应的最高价氧化物的水化物的酸性减弱.
B.电子排布相同的离子,原子序数越大,半径越小;
C.同主族从上到下金属性增强,失电子能力增强;
D.同主族从上到下非金属性减弱,对应的最高价氧化物的水化物的酸性减弱.
解答:
解:A.原子不带电,分子也不带电,则在分子中质子数等于核外电子数,故A错误;
B.电子排布相同的离子,原子序数越大,半径越小,原子序数:O<F,则半径O2->F-,故B错误;
C.同主族从上到下金属性增强,失电子能力增强,Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强,故C正确;
D.同主族从上到下非金属性减弱,对应的最高价氧化物的水化物的酸性减弱,非金属性:P>As,则H3PO4酸性比H3AsO4的强,故D错误.
故选C.
B.电子排布相同的离子,原子序数越大,半径越小,原子序数:O<F,则半径O2->F-,故B错误;
C.同主族从上到下金属性增强,失电子能力增强,Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强,故C正确;
D.同主族从上到下非金属性减弱,对应的最高价氧化物的水化物的酸性减弱,非金属性:P>As,则H3PO4酸性比H3AsO4的强,故D错误.
故选C.
点评:本题考查了原子结构、元素周期表的结构和元素周期律的应用,周期表中周期与周期之间,族与族之间含有较多规律,在学习中要善于抓住这些规律会起到事半功倍的效果,题目难度不大.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:对上述流程中的判断正确的是( )
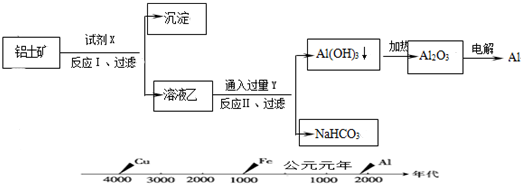

| A、试剂X为稀硫酸 |
| B、反应Ⅱ中生成Al(OH)3的反应为:CO2+2AlO2-+3H2O═2Al(OH)3↓+CO32- |
| C、人类对金属的使用历史与金属活动顺序和冶炼的难易程度有关 |
| D、Al2O3熔点很高,电解耗能大,可采用电解熔融AlCl3冶炼Al |
25℃、101kPa下,1mol氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
| A、2H2(g)+O2(g)=2H2O(1)△H=-285.8kJ/mol |
| B、2H2(g)+O2(g)=2H2O(1)△H=+571.6 kJ/mol |
| C、2H2(g)+O2(g)=2H2O(g)△H=-571.6 kJ/mol |
| D、H2(g)+O2(g)=H2O(1)△H=-285.8kJ/mol |
下列说法正确的是( )
| A、共价化合物中可能含有离子键 |
| B、区别离子化合物和共价化合物的方法是看其水溶液是否能够导电 |
| C、离子化合物中只含有离子键 |
| D、离子化合物熔融状态能电离出自由移动的离子,而共价化合物不能 |
设NA表示阿伏加德罗常数值,下列叙述正确的是( )
| A、常温常压下,56 g Fe与足量的盐酸完全反应转移的电子数为3NA |
| B、标准状态下,11.2 L氯气含有分子数为0.5 NA |
| C、0.1 mol?L-1的硫酸铝溶液所含的SO42-数就是0.3NA |
| D、NA个He分子所具有的体积为22.4L |
下列离子方程式正确的是( )
| A、三氯化铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ |
| B、向含有0.2 mol FeI2的溶液中通入0.25 mol Cl2:8I-+2Fe2++5Cl2═10Cl-+4I2+2Fe3+ |
| C、K37ClO3与浓盐酸(HCl)在加热时生成Cl2:37ClO3-+6HCl═37Cl-+3Cl2↑+3H2O |
| D、将0.1 mol/L盐酸数滴缓缓滴入0.1 mol/L 25 mL Na2CO3溶液中,并不断搅拌:2H++CO32-═CO2↑+H2O |