题目内容
实验室用6.5克锌粒与足量的稀硫酸反应可以制取标准状况下氢气多少升?
考点:化学方程式的有关计算
专题:
分析:根据n=
计算Zn的物质的量,发生反应:Zn+H2SO4═ZnSO4+H2↑,根据方程式计算生成氢气的物质的量,再根据V=nVm计算氢气的体积.
| m |
| M |
解答:
解:6.5g Zn的物质的量为
=0.1mol
设生成氢气物质的量为x,则:
Zn+H2SO4═ZnSO4+H2↑
1 1
0.1mol x
所以x=
=0.1mol,
故标况下生成氢气体积为0.1mol×22.4L/mol=2.24L,
答:标况下生成氢气体积为2.24L.
| 6.5g |
| 65g/mol |
设生成氢气物质的量为x,则:
Zn+H2SO4═ZnSO4+H2↑
1 1
0.1mol x
所以x=
| 0.1mol×1 |
| 1 |
故标况下生成氢气体积为0.1mol×22.4L/mol=2.24L,
答:标况下生成氢气体积为2.24L.
点评:本题考查化学方程式有关计算,比较基础,注意对化学方程式意义理解,有利于基础知识的巩固.

练习册系列答案
相关题目
下列有关说法不正确的是( )
| A、铝制品比铁制品在空气中更容易被腐蚀 |
| B、实验室用铜片与稀硝酸反应产生的气体可用排水法收集 |
| C、向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加氨水现象相同 |
| D、以海水为原料能制取Na、HCl、Mg、Br2等物质 |
下列说法正确的是( )
| A、只有在原子中,质子数才与核外电子数相等 |
| B、O2-半径比F-的小 |
| C、Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 |
| D、P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的弱 |
某些化学概念在逻辑上存在下图所示关系,则下列说法中正确的是:( )

| A、纯净物(B)与混合物(A)属于包含关系 |
| B、化合物(B)与氧化物(A)属于包含关系 |
| C、单质与化合物属于交叉关系 |
| D、氧化反应与化合反应属于并列关系 |
下列说法正确的是( )
| A、16O2与18O2互为同位素,H2O、D2O、T2O互为同素异形体,N60和N2互为同系物 |
| B、除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| C、非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 |
D、Ca的原子结构示意图为 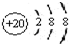 |
下列说法中正确的是( )
| A、1mol任何纯净物都含有相同的原子数 |
| B、1molO2中约含有6.02×1023个氧分子 |
| C、1mol水中含有8mol电子 |
| D、阿伏加德罗常数就是6.02×1023mol-1 |
1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献.他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化.下列说法正确的是( )
| A、化学不做实验,就什么都不知道 |
| B、化学不再需要实验 |
| C、化学不再是纯实验科学 |
| D、未化学的方向是经验化 |
某种溶质的溶液的pH=2,向该溶液中加水到体积变为原来溶液体积的10倍,所得溶液的pH在2-3之间,则溶液中的溶质可能是 ①强酸 ②弱酸 ③强酸弱碱盐 ④强碱弱酸盐( )
| A、②④ | B、②③ | C、③④ | D、①② |
已知:甲+H2O→乙+丙,根据以上反应式进行的下列推断不合理的是( )
| A、甲为Fe丙为 Fe2O3 |
| B、甲为F2丙为O2 |
| C、甲为KH丙为 H2 |
| D、甲为CaC2丙为C2H2 |