题目内容
2.将0.040mol•L-1的HCN与0.020mol•L-1 NaOH溶液等体积混合,已知该混合溶液中c (Na+)>c (CN-),则c (HCN)>c (CN-)(用“>”、“<”、“=”符号填空).分析 将0.040mol•L-1的HCN与0.020mol•L-1 NaOH溶液等体积混合,反应后溶质为等浓度的HCN和NaCN,根据物料守恒可得:2c (Na+)=c(HCN)+c (CN-),然后结合c (Na+)>c (CN-)判断c (HCN)与c (CN-)的浓度大小.
解答 解:将0.040mol•L-1的HCN与0.020mol•L-1 NaOH溶液等体积混合,反应后溶质为等浓度的HCN和NaCN,反应后的溶液中存在物料守恒可得:2c (Na+)=c(HCN)+c (CN-),由于c (Na+)>c (CN-),则c (HCN)>c (Na+)>c (CN-),
故答案为:>.
点评 本题考查了离子浓度大小比较,题目难度不大,明确反应后溶质组成为解答关键,注意掌握物料守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.在一密闭容器中进行2SO2+O2?2SO3三氧化硫的反应,己知反应过程中某一时刻的数据是:SO2、O2、SO3的浓度分别是0.2mol/L、0.1mol/L、0.2mol/L,当达到平衡时可能数据是和( )
| A. | SO2 0.4mol/L | B. | SO2 0.25mol/L | ||
| C. | SO2 和SO3均为0.15mol/L | D. | O2 0.2mol/L |
10.短周期元素X、Y、Z在周期表中的位置如图所示,则下列说法正确的是( )


| A. | Z的最高价氧化物的水化物是强酸 | |
| B. | Y的最高价氧化物的水化物是一种强酸 | |
| C. | Z离子半径比Y原子半径小 | |
| D. | Z的气态氢化物比Y的气态氢化物稳定 |
17.咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为有关咖啡酸的说法中不正确的是( )
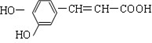

| A. | 咖啡酸可以发生还原、取代、加聚等反应 | |
| B. | 1 mol咖啡酸最多能消耗3 mol的NaHCO3 | |
| C. | 1 mol咖啡酸可与4 mol H2 发生加成反应 | |
| D. | 咖啡酸与FeCl3 溶液可以发生显色反应 |
7.下列有关元素化合物的叙述正确的是( )
| A. | 钠在空气中燃烧生成淡黄色的氧化钠固体 | |
| B. | 盛有氯气的集气瓶中加入干燥有色布条后,C12可以使有色布条褪色 | |
| C. | 检验FeCl2溶液中的少量Fe3+,可以用KSCN溶液 | |
| D. | C60、金刚石、石墨都是碳的同素异形体,它们之间的转化属于物理变化 |
14.下列化合物中,属于盐的是( )
| A. | NH3 | B. | KOH | C. | H2SO4 | D. | NaClO |
11.25℃时,10mL 0.1mol•L-1 的一元酸HA溶液,在水中约有0.1%发生电离(每1000个HA只有1个HA电离),下列叙述不正确的是( )
| A. | 该溶液的pH约是4 | |
| B. | HA一定是一种弱酸 | |
| C. | 恰好中和时消耗NaOH的物质的量是10-6mol | |
| D. | 与足量Mg完全反应生成标准状况下气体的体积可能是11.2 mL |
