��Ŀ����
15����ͼΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��ش��������⣺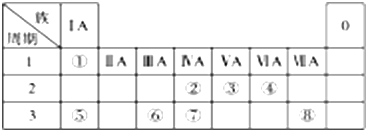
��1���ؿ��к�����ߵĽ���Ԫ�آ������ڱ��е�λ���ǵ�3���ڢ�A�壮
��2�����γɵĵ�����ˮ��Ӧ�����ӷ���ʽΪCl2+H2O
 HClO+H++Cl-��
HClO+H++Cl-����3���ڢߵķǽ�����ǿ����ͨ���Ƚ�������Ԫ��ac�����ţ�
a��ԭ�ӵĵõ��ӵ����� b�������������
c����̬�⻯����ȶ��� d�����ʵ��۷е�
��4��д��һ���ɢܢݢ�Ԫ���γɵļȺ������Ӽ��ֺ��й��ۼ������ʵĵ���ʽ
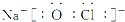 ��
����5��Ԫ�آ�����γɵĻ������������ӻ��������ӻ�����������ۻ���������õ���ʽ��ʾ�û�������γɹ��̣�
 ��
��
���� �ɶ�����Ԫ�������ڱ���λ�ÿ�֪���١���ֱ�ΪH��C��N��O��Na��Al��Si��Cl��
��1����ΪAl��
��2��������ˮ��Ӧ���������HClO��
��3�������⻯����ȶ��ԡ���ۺ���������ԡ��õ��������ȱȽϷǽ����ԣ�
��4���ɢܢݢ�Ԫ���γɵļȺ������Ӽ��ֺ��й��ۼ�������NaClO��
��5��Ԫ�آ�����γɵĻ�����ΪNaCl��Ϊ���ӻ����
��� �⣺�ɶ�����Ԫ�������ڱ���λ�ÿ�֪���١���ֱ�ΪH��C��N��O��Na��Al��Si��Cl��
��1���ؿ��к�����ߵĽ���Ԫ�آ������ڱ��е�λ���ǵ�3���ڢ�A�壬�ʴ�Ϊ����3���ڢ�A�壻
��2�����γɵĵ�����ˮ��Ӧ�����ӷ���ʽΪCl2+H2O HClO+H++Cl-���ʴ�Ϊ��Cl2+H2O
HClO+H++Cl-���ʴ�Ϊ��Cl2+H2O HClO+H++Cl-��
HClO+H++Cl-��
��3��a��ԭ�ӵĵõ��ӵ������ɱȽϷǽ����ԣ���aѡ��
b������������Բ�һ��Ϊ��ۺ����ᣬ���ܱȽϷǽ����ԣ���b��ѡ��
c���ǽ�����Խǿ����Ӧ�⻯��Խ�ȶ�������̬�⻯����ȶ��ԿɱȽϷǽ����ԣ���cѡ��
d�����ʵ��۷е㣬Ϊ�������ʣ����ܱȽϷǽ����ԣ���d��ѡ��
�ʴ�Ϊ��a c��
��4���ɢܢݢ�Ԫ���γɵļȺ������Ӽ��ֺ��й��ۼ�������NaClO�������ʽΪ 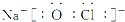 ��
��
�ʴ�Ϊ��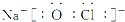 ��
��
��5��Ԫ�آ�����γɵĻ�����ΪNaCl��Ϊ���ӻ�����õ���ʽ��ʾ�û�������γɹ���Ϊ ��
��
�ʴ�Ϊ�����ӻ���� ��
��
���� ���⿼��λ�á��ṹ�����ʵĹ�ϵ��Ϊ��Ƶ���㣬����Ԫ�ص�λ�á����ʡ�Ԫ�ػ�����֪ʶΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�⻯ѧ���P������֪ʶ��Ӧ�ã���Ŀ�ѶȲ���

| A�� | ԭ�Ӱ뾶X��Y��Z | B�� | ��̬�⻯���ȶ��� HX��HZ��HY | ||
| C�� | �ǽ�����X��Y��Z | D�� | ��̬�⻯�ﻹԭ��HX��HY��HZ |

| A�� | ������������Һ�����ʵ���Ũ��Ϊ0.1 mol/L | |
| B�� | ��b�㣬c ��Na+���Tc��CH3COO-�� | |
| C�� | ��d�㣬��Һ����������Ũ���ɴ�С��˳��Ϊc ��CH3COO-����c ��H+ ����c ��Na+����c ��OH-�� | |
| D�� | ����������Һ�������Һǡ����ȫ��Ӧ�ĵ�λ������b��d���ij�� |
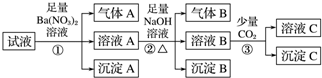
| A�� | ԭ��Һ��һ����Fe2+��SO42-��H+��NH4+��Al3+ | |
| B�� | ԭ��Һ��һ��û��Ba2+��CO32-��NO3- | |
| C�� | ������з�Ӧ�����ӷ���ʽΪ2AlO-+CO2+3H2O�T2Al��OH��3��+CO32- | |
| D�� | ����A��B֮��϶����ܷ�����Ӧ |
 �о������ḻ��CO2��ȫ������Ϊ��̼Դ�������ǰӦ����㷺��̼Դ��ʯ�ͺ���Ȼ��������������Ҷ���ݽߵ�Σ����ͬʱ�ֿɻ�����CO2�ۻ�������������ЧӦ��ʵ��CO2������ѭ����
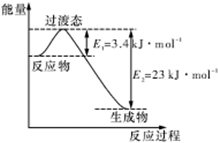
�о������ḻ��CO2��ȫ������Ϊ��̼Դ�������ǰӦ����㷺��̼Դ��ʯ�ͺ���Ȼ��������������Ҷ���ݽߵ�Σ����ͬʱ�ֿɻ�����CO2�ۻ�������������ЧӦ��ʵ��CO2������ѭ������1��Ŀǰ��ҵ����һ�ַ�������CO2��H2��230����������������ת�����ɼ״�������ˮ��������ͼ��ʾ��ѹ������0.5mol CO2��1.5mol H2ת���ʴ�80%ʱ�������仯ʾ��ͼ�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������bd������ĸ����
a��������ѹǿ����
b��H2�������������
c��c��H2��=3c��CH3OH��
d���������ܶȲ���
e��2��C=O���ѵ�ͬʱ��6��H-H����
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO��g��+H2O��g��?CO2��g��+H2��g�����õ������������ݣ�
| ʵ���� | �¶� �� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a/b��ֵ�������ֵ��ȡֵ��Χ����
��ʵ��4����900��ʱ���ڴ������м���CO��H2O��CO2��H2��Ϊ1mol�����ʱv��������v���棩�������������������=��������
��3����֪�ڳ��³�ѹ�£�
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=-1275.6kJ/mol
��2CO��g��+O2��g��=2CO2��g����H=-566.0kJ/mol
��H2O��g��=H2O��l����H=-44.0kJ/mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽCH3OH��l��+O2��g��=CO��g��+2H2O��l����H=-442.8kJ/mol
��4����֪������һ�ֶ�Ԫ���ᣬ�������ƣ�NaHC2O4����Һ�����ԣ������£���10mL 0.0l mol��L-l H2C2O4��Һ�еμ�10mL 0.01mol��L-l NaOH��Һʱ���Ƚ���Һ�и�������Ũ�ȵĴ�С��ϵc��Na+����c��HC2O4-����c��H+����c��C2O42-����c��OH-����
��5���Լ��ѡ�����������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�أ��õ�صĸ�����Ӧʽ
ΪCH3OCH3+16OH--12e-=2CO32-+11H2O��
| A�� | ��0.1 mol•L-1��CH3COOH��Һ�м�������̼��ƹ��壬��Һ��pH���� | |
| B�� | �����£�pH=4��NaHSO4��Һ�У�ˮ�������H+Ũ��Ϊ1��10-10 mol•L-1 | |
| C�� | Ũ�Ⱦ�Ϊ0.1 mol•L-1��HCN��Һ��NaCN��Һ�������ϣ���������仯������Һ��c��HCN��+c��CN-��=0.1 mol•L-1 | |
| D�� | pH��ͬ�Ģ�NH4Cl����NH4Al��SO4��2���ۣ�NH4��2SO4������Һ��c��NH${\;}_{4}^{+}$�����ڣ��ۣ��� |
| A�� | �й��Ŵ�����������Һ���������ͭ�������ͭ�� | |
| B�� | ���ð�˾ƥ�ֳ���ˮ���ᷴӦʱ����NaHCO3��Һ�ⶾ | |
| C�� | ʯ���ѽ⡢ú�ĸ��������ƴ��������ʵı��Ժ����������ӵľۼ����ǻ�ѧ�仯 | |
| D�� | ȼ�ϵ������ѵ���SO2�Ļ������ú�NOx�Ĵ�ת�����Ǽ�����������Ĵ�ʩ |