题目内容
4.广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质.根据上述观点,下列说法正确的是( )| A. | CaO2的水解产物是Ca(OH)2和H2O2 | B. | NaClO的水解产物之一是HClO | ||
| C. | PCl3的水解产物是PH3和HClO | D. | Mg3N2水解生成NH3和Mg(OH)2 |
分析 水解是反应中各物质和水分别解离成两部分、然后两两重新组合成新的物质,该反应相当于复分解反应,反应过程中没有电子转移,其特征是没有元素化合价升降,据此分析解答.
解答 解:水解是反应中各物质和水分别解离成两部分、然后两两重新组合成新的物质,该反应相当于复分解反应,反应过程中没有电子转移,其特征是没有元素化合价升降,
A.CaO2的水解产物是Ca(OH)2和H2O2,该反应中没有元素化合价升降,符合水解原理,故A不选;
B.该反应中元素化合价不变,NaClO生成HClO和NaOH,符合水解原理,故B不选;
C.该反应中Cl元素化合价由-1价变为+1价,有电子转移,不符合水解原理,故C选;
D.Mg3N2与水反应的产物是NH3和Mg(OH)2,该反应中没有元素化合价升降,符合水解原理,故D不选;
故选C.
点评 本题考查了水解原理,正确理解题干信息是解本题关键,再结合元素化合价是否变化分析解答,题目难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
19.高温高压下,1L密闭容器中,发生如下反应:2H2+CO?CH3OH.反应开始时H2的物质的量为5mol,5min时变为0.5mol,则5min内该反应的平均反应速率v(H2) (单位:mol.L-1.min-1)为( )
| A. | 9.0 | B. | 0.9 | C. | 0.45 | D. | 4.5 |
9.下列物质不能与金属钠反应的是( )
| A. | 水 | B. | 煤油 | C. | 盐酸 | D. | 乙醇 |
16.历史上发现元素周期律的化学家是( )
| A. | 法拉第(英国) | B. | 凯库勒(德国) | C. | 门捷列夫(俄国) | D. | 道尔顿(英国) |
13.下列电离方程式正确的是( )
| A. | NH3•H2O═NH4++OH- | B. | H2S?S2-+2H+ | ||
| C. | CaCO3?Ca2++CO32- | D. | CH3COONH4═CH3COO-+NH4+ |
14.下列物质中具含离子键又含共价键的是( )
| A. | HCl | B. | Cl2 | C. | Na2O2 | D. | NaOH |
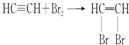
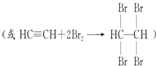 .
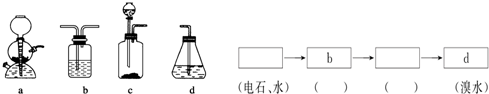
.
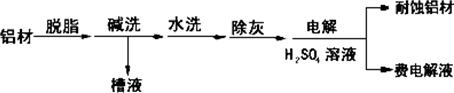
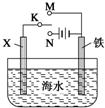 对金属制品进行抗腐蚀处理,可延长其使用寿命.
对金属制品进行抗腐蚀处理,可延长其使用寿命.