题目内容
17.阿佛加德罗常数符号为NA,下列叙述正确的是( )| A. | 22.4LL任何气体都约含NA个气体分子 | |
| B. | 标准状况下,1mol液溴的体积约为22.4L | |
| C. | 1mol铁与足量盐酸反应,转移电子数为3NA | |
| D. | 18gNH4+中含有的电子数为10NA |
分析 A.气体状况为定,Vm不确定;
B.气体摩尔体积使用对象为气体;
C.铁与盐酸反应生成氯化亚铁;
D.质量转化为物质的量,结合1个氨根离子含有10个电子解答.
解答 解:A.气体状况为定,Vm不确定,无法计算22.4L气体的物质的量,无法计算所含分子数,故A错误;
B.标况下,液溴为液体,不能使用气体摩尔体积,故B错误;
C.1mol铁与足量盐酸反应生成1mol氯化亚铁,转移电子数为2NA,故C错误;
D.18gNH4+中含有的电子数为$\frac{18g}{18g/mol}$×10×NA=10NA,故D正确;
故选:D.
点评 本题考查物质的量的有关计算,为高频考点,侧重考查学生判断及计算能力,明确以物质的量为核心计算公式,熟悉气体摩尔体积使用条件和对象是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.设NA表示阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 200g63%的浓硝酸中含氧原子个数为6NA | |
| B. | 50mL12mol•L-1 盐酸和足量MnO2共热,转移的电子数目为0.3NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标况下)气体时,电路中通过的电子数目为4NA | |
| D. | 若CH3COONa溶液中CH3COO-的数目为6NA,则Na+的目为6NA |
8.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.2NA | |
| B. | 2 L 0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 18g H2O含有10NA个质子 | |
| D. | 标准状况下,11.2L苯中含有分子的数目为0.5NA |
5.原子结构的有关数据中,不符合Cl<Br<I的变化规律的是( )
| A. | 电子层数 | B. | 原子核内质子数 | C. | 原子半径 | D. | 最外层电子数 |
12.实现下列变化,不需要破坏化学键的是( )
| A. | 氯化氢气体溶于水 | B. | 溴蒸气被木炭吸附 | ||
| C. | 加热氯酸钾使其分解 | D. | 氯化钠熔融 |
9.物质的量的浓度的单位是( )
| A. | g/L | B. | mol/L | C. | g/mol | D. | mol |
6.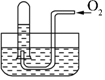 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )| A. | 可能是N2与NO2的混合气体 | B. | 可能是O2与NO2的混合气体 | ||
| C. | 一定是NO与NO2的混合气体 | D. | 只可能是NO2一种气体 |
8.反应Cu2++Zn=Cu+Zn2+可在溶液中进行完全,由该反应可判断Cu2+的氧化性强于( )
| A. | Zn | B. | Cu | C. | Zn2+ | D. | Cu+ |
 ;
;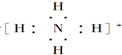 ;
;