题目内容
按照阿伏加德罗定律,下列叙述不正确的( )
| A、同温同压下两种气体的体积之比等于物质的量之比 |
| B、同温同压下两种气体的物质的量之比等于密度之比 |
| C、同温同压下两种气体的密度之比等于摩尔质量之比 |
| D、同温同体积下两种气体的物质的量之比等于压强之比 |
考点:阿伏加德罗定律及推论
专题:
分析:同温同压下,气体摩尔体积相等,根据V=nVm、ρ=
、同温条件下气体的物质的量与其压强成正比进行判断.
| M |
| Vm |
解答:
解:A.同温同压下,气体摩尔体积相等,根据V=nVm知,气体的体积之比等于其物质的量之比,故A正确;
B.同温同压下,气体摩尔体积相等,根据ρ=
知,气体的密度之比等于摩尔质量之比,与物质的量无关,故B错误;
C.根据B知,相同条件下气体的密度之比等于其摩尔质量之比,故C正确;
D.同温条件下气体,它们的物质的量与其压强成正比,所以同温同体积下两种气体的物质的量之比等于压强之比,故D正确;
故选B.
B.同温同压下,气体摩尔体积相等,根据ρ=
| M |
| Vm |
C.根据B知,相同条件下气体的密度之比等于其摩尔质量之比,故C正确;
D.同温条件下气体,它们的物质的量与其压强成正比,所以同温同体积下两种气体的物质的量之比等于压强之比,故D正确;
故选B.
点评:本题考查阿伏伽德罗定律及其推论,侧重考查基本理论的推导,明确物质的量公式中各个物理量的关系是解本题关键,注意有关气体体积的计算中前提条件,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
下列各物质既能与强酸反应,又能与强碱反应的是( )
①Na2SO4;②AlCl3;③Al(OH)3;④Al2O3;⑤NaHCO3.
①Na2SO4;②AlCl3;③Al(OH)3;④Al2O3;⑤NaHCO3.
| A、①②③④⑤ | B、①②④⑤ |
| C、②④⑤ | D、③④⑤ |
 在密闭容器中发生反应:X+3Y═2Z(该反应放热),其中Z呈气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图.下列判断正确的是( )
在密闭容器中发生反应:X+3Y═2Z(该反应放热),其中Z呈气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图.下列判断正确的是( )| A、T1大于T2 |
| B、Y一定呈气态 |
| C、升高温度,该反应的正反应速率减小 |
| D、当n(X):n(Y):n(Z)=1:3:2时,反应一定达到平衡状态 |
下列变化规律错误的是( )
| A、微粒半径:F-<Cl-<Br -<I- |
| B、稳定性:HI<HBr<HCl<HF |
| C、沸点:HF<HCl<HBr<HI |
| D、阴离子还原性:F-<Cl -<Br -<I - |
在一可压缩的密闭容器中,发生可逆反应:M(g)+N(?)P(g)+Q(g)△H>0,当压缩体积时,M的转化率不变.在其它条件不变的情况下,采用以下措施使M的转化率增大( )
| A、加入一定量的M |
| B、加入一定量的不与M、N、P、Q反应的气体 |
| C、反应温度升高 |
| D、加入某物质作催化剂 |
下列说法不正确的是( )
| A、使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 |
| B、石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
| C、向汽油中添加甲醇后,该混合燃料的热值不变 |
| D、利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法 |
用酸性氢氧燃料电池为电源进行电解的实验装置如图所示.下列说法正确的是( )
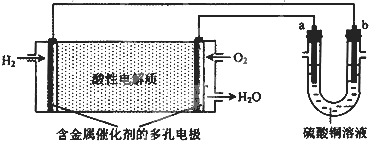

| A、a为负极,b为正极 |
| B、若a极是铁,b极是铜,b极逐渐溶解,a极上有铜析出 |
| C、若a、b极都是石墨,在相同条件下,理论上a极产生的气体与电池中消耗的O2体积相等 |
| D、若电解精炼粗铜时,b极是粗铜,a极是纯铜 |
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、1g氢气中所含有的分子数为NA |
| B、0.5mol/L的AlCl3溶液中含有氯离子数为1.5NA |
| C、27g铝与足量NaOH反应消耗OH-的数目为4NA |
| D、7.8g的Na2O2与水完全反应转移的电子数目为0.1NA |