题目内容
17.判断物质在不同溶剂中的溶解性时,一般都遵循“相似相溶”规律.下列装置中,不宜用做HCl尾气吸收的是( )| A. |  | B. |  | C. | 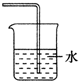 | D. | 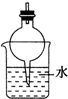 |
分析 HCl是极性分子,水是极性分子,四氯化碳是非极性分子,据此解题.
解答 解:HCl是极性分子,水是极性分子,四氯化碳是非极性分子,氯化氢易溶于水,难溶于四氯化碳.
A.倒置的漏斗可防倒吸,故A错误;
B.氯化氢难溶于四氯化碳,可防倒吸,故B错误;
C.氯化氢易溶于水,会发生倒吸,故C正确;
D.大肚瓶生防止倒吸,故D错误.
故选C.
点评 本题考查尾气处理装置,注意根据“相似相溶”规律解题,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列事实能说明亚硝酸是弱电解质的是( )
①25℃时亚硝酸钠溶液的pH大于7 ②用HNO2溶液做导电试验,灯泡很暗
③HNO2溶液不与Na2SO4溶液反应 ④0.1mol•L-1HNO2溶液的pH=2.1.
①25℃时亚硝酸钠溶液的pH大于7 ②用HNO2溶液做导电试验,灯泡很暗
③HNO2溶液不与Na2SO4溶液反应 ④0.1mol•L-1HNO2溶液的pH=2.1.
| A. | ①②③ | B. | ②③④ | C. | ①④ | D. | ② |
8.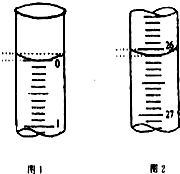 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化.直到因加入一滴盐酸后,溶液由黄色变为橙色,并半分钟内不复原为止.
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示:所用盐酸溶液的体积为26.10mL.
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是C
(A)酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
(B)滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
(C)读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(D)酸式滴定管在滴定前有气泡,滴定后气泡消失
(4)某学生根据三次实验分别记录有关数据如表:请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:(NaOH)=0.1044mol/L(保留小数点后4位).
 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化.直到因加入一滴盐酸后,溶液由黄色变为橙色,并半分钟内不复原为止.
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示:所用盐酸溶液的体积为26.10mL.
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是C
(A)酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
(B)滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
(C)读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(D)酸式滴定管在滴定前有气泡,滴定后气泡消失
(4)某学生根据三次实验分别记录有关数据如表:请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:(NaOH)=0.1044mol/L(保留小数点后4位).
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
5.2015年9月16日某市一家无证照工厂因废水向外直排被查,检测结果显示,该长所排污水中铜超标300倍.
(1)在该厂所排污水中放置细铁网可获得金属铜,其原理是Fe+Cu2+=Fe2++Cu(用离子方程式表示).
(2)铜超标污水中还可能大量存在的阴离子是C、D.
A.CO32- B.OH- C.Cl- D.SO42-
(3)检测部门对该厂所排废水的检测数据如下:
①该厂所排污水中铜离子的浓度是0.066mol•L-1;
②若要使该厂废水排放达标,应控制的最小pH=9.2.(已知25℃时,Ksp[Cu(OH)2]=2.2×10-20)
(4)该厂废水可以“变废为宝”,其流程图如下:

①高浓度的含铜废水经蒸发浓缩、冷却结晶、过滤、洗涤、干燥可以得到纯度较高的铜盐晶体.
②用较高浓度含铜废水点解制铜,其阴极的电极反应式是Cu2++2e-=Cu;电解5L该厂排放的含铜废水,理论上可以得到铜21.12g.
(1)在该厂所排污水中放置细铁网可获得金属铜,其原理是Fe+Cu2+=Fe2++Cu(用离子方程式表示).
(2)铜超标污水中还可能大量存在的阴离子是C、D.
A.CO32- B.OH- C.Cl- D.SO42-
(3)检测部门对该厂所排废水的检测数据如下:
| 次数 | 测量项目 | 测量数据(mg/mL) |
| 1 | 铜离子含量 | 4.224 |
| 2 | 4.225 | |
| 3 | 4.223 | |
| 4 | 2.005 |
②若要使该厂废水排放达标,应控制的最小pH=9.2.(已知25℃时,Ksp[Cu(OH)2]=2.2×10-20)
(4)该厂废水可以“变废为宝”,其流程图如下:

①高浓度的含铜废水经蒸发浓缩、冷却结晶、过滤、洗涤、干燥可以得到纯度较高的铜盐晶体.
②用较高浓度含铜废水点解制铜,其阴极的电极反应式是Cu2++2e-=Cu;电解5L该厂排放的含铜废水,理论上可以得到铜21.12g.
6.下表是元素周期表的一部分,针对表中的①~=10 ⑩种元素,填写下列空白:
(1)写出下列元素的名称⑧氩⑩钙
(2)在①~⑩元素中,金属性最强的元素是K(填元素符号),气态氢化物能与其最高价氧化物对应的水化物发生反应生成盐的元素是N(填元素符号).
(3)元素⑥与元素⑦相比,⑦的非金属性较强,下列表述中能证明这一事实的是bd.
a.常温下⑥的单质和⑦的单质状态不同
b.⑦的氢化物比⑥的氢化物稳定
c.一定条件下⑥和⑦的单质都能与氢氧化钠溶液反应
d.一定条件下⑥和⑦的单质与Fe反应的产物不同
(4)⑤的单质可以与⑨的最高价氧化物的水化物的溶液反应,若将该反应设计成原电池,其负极的电极反应式Al-3e-+4OH-=AlO2-+2H2O.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 | |
| 第2周期 | ① | ② | ③ | |||||
| 第3周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 第4周期 | ⑨ | ⑩ |
(2)在①~⑩元素中,金属性最强的元素是K(填元素符号),气态氢化物能与其最高价氧化物对应的水化物发生反应生成盐的元素是N(填元素符号).
(3)元素⑥与元素⑦相比,⑦的非金属性较强,下列表述中能证明这一事实的是bd.
a.常温下⑥的单质和⑦的单质状态不同
b.⑦的氢化物比⑥的氢化物稳定
c.一定条件下⑥和⑦的单质都能与氢氧化钠溶液反应
d.一定条件下⑥和⑦的单质与Fe反应的产物不同
(4)⑤的单质可以与⑨的最高价氧化物的水化物的溶液反应,若将该反应设计成原电池,其负极的电极反应式Al-3e-+4OH-=AlO2-+2H2O.

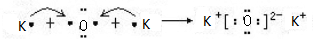

 .
.