题目内容
7.现有NH3、F2、Cl2、Na、Fe、Na2O、Na2O2、SO2、CO2、NO2等中学化学常见物质,根据它们与水是否发生氧化还原反应进行分类.请回答下列问题:
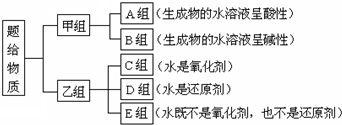
(1)该种分类方法叫作树状分类法.
(2)淡黄色固体位于E组(填“A~E”).
(3)A组中溶解度较大的物质使溴水褪色的原因是其具有还原性.
(4)C组中某一物质须在加热时才能与水蒸气反应,其化学方程式为4H2O(g)+3Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2.
(5)用化学方程式表示B组中气体物质的实验室制法Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(6)D组中的物质是F2.
分析 (1)由分类的角度可知为树状分类法;
(2)淡黄色固体为Na2O2;
(3)A组中溶解度较大的物质为SO2,使溴水褪色发生氧化还原反应,体现还原性;
(4)C组中某一物质须在加热时才能与水蒸汽反应,应为Fe;
(5)B组中水溶液呈碱性,气体物质是氨气,实验室制法Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(6)氟气与水反应氟气是氧化剂,水是还原剂.
解答 解:(1)由分类的角度可知为树状分类法,
故答案为:树状分类法;
(2)淡黄色固体为Na2O2,故答案为:E;
(3)A组中溶解度较大的物质为SO2,使溴水褪色发生氧化还原反应,体现还原性,
故答案为:还原性;
(4)C组中某一物质须在加热时才能与水蒸汽反应,应为Fe,反应的方程式为4H2O(g)+3Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,
故答案为:4H2O(g)+3Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
(5)B组中水溶液呈碱性,气体物质是氨气,实验室制法Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;(6)氟气与水反应氟气是氧化剂,水是还原剂,故答案为:F2.
点评 本题综合考查氧化还原反应知识以及物质的分类,侧重于学生的分析能力和物质的性质的综合考查,为高考常见题型,注意把握题给信息结合元素化合价的角度分析,难度不大.

| A. | 所得溶液中C(Fe2+):C(Fe3+)=1:1 | B. | 所得溶液中C(NO3-)=2.75mol/L | ||
| C. | 反应后生成NO的体积为28 L | D. | 所得溶液中溶质只有FeSO4和K2SO4 |

| A. | 蔗糖变黑体现了浓硫酸的脱水性 | |
| B. | 蔗糖体积膨胀变成疏松多孔的海绵状物质炭 | |
| C. | 实验中有大量气体产生体现了浓硫酸的强酸性 | |
| D. | 将产生的气体通入品红溶液,溶液会褪色 |
| A. | -(12-3n) | B. | -(12-5n) | C. | -(6-3n) | D. | -(10-n) |


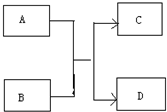 运用有关知识,回答下列问题.
运用有关知识,回答下列问题.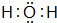 ,实验室中检验C的试剂及现象是湿润的红色石蕊试纸变蓝色.
,实验室中检验C的试剂及现象是湿润的红色石蕊试纸变蓝色.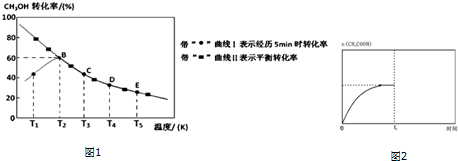
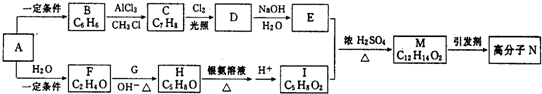
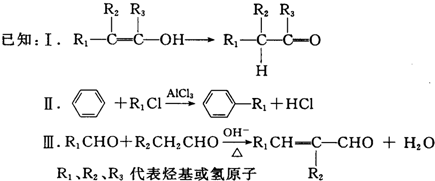
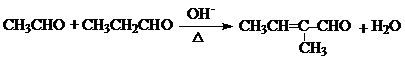 .
.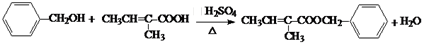 .
.