题目内容
2.物质在下列应用中,利用了其还原性的是( )| A. | 纯碱去油污 | B. | 铝冶炼金属 | C. | 硝酸制炸药 | D. | 漂粉精漂白织物 |
分析 氧化还原反应中元素化合价升高作还原剂,表现还原性,据此分析.
解答 解:A.纯碱去油污,纯碱水解显碱性,油脂在碱性条件下水解,没有发生氧化还原反应,故A不选;
B.铝冶炼金属,铝作还原剂把金属由化合物中置换出来,铝作还原剂,利用了其还原性,故B选;
C.硝酸制炸药,生成三硝基甲苯,没有发生氧化还原反应,故C不选;
D.漂粉精漂白织物,表现了次氯酸钙的强氧化性,故D不选;
故选B.
点评 本题考查氧化还原反应,把握元素的化合价与微粒性质的关系为解答的关键,侧重氧化性、还原性的考查,注意从元素的化合价角度分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.在光照条件下,CH4与Cl2能发生取代反应:若将1 mol CH4与Cl2反应,待反应完成后测得四种有机取代物的物质的量之比为:n(CH3Cl):n(CH2Cl2):n(CHCl3):n(CCl4)=4:3:2:1,则消耗的Cl2为( )
| A. | 1.0 mol | B. | 2.0 mol | C. | 3.0 mol | D. | 4.0 mol |
17.以下化学方程式中水只作为氧化剂的是( )
| A. | NaH+H2O═NaOH+H2↑ | B. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | ||
| C. | F2+H2O═2HF+O2↑ | D. | Cl2+H2O?HCl+HClO |
7.下列各组数据比较,前者比后者小的是( )
| A. | 氯水与氨水中微粒种类 | B. | 乙烷与苯分子中碳碳键键长 | ||
| C. | 氯化铯与氯化钠的熔点 | D. | Al2O3与AlCl3的熔点 |
14.对有关NaClO和NaCl混合溶液的叙述正确的是( )
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,K+、OH-、S2-、NO3-不能大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,离子方程式为:2Fe2++ClO-+2H+→Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
11.下列实验操作可以达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 鉴别蚕丝制品和羊毛制品 | 用灼烧方法验证,闻是否有烧焦羽毛气味 |
| B | 检验淀粉水解的最终产物的还原性 | 取少量淀粉溶液,与稀硫酸共热后再加入银氨溶液,水浴加热,观察是否出现银镜 |
| C | 检验氯仿(CHCl3)中的氯元素 | 取少量氯仿加入硝酸银溶液,观察是否出现白色沉淀 |
| D | 除去乙酸乙酯中混有的少量乙酸 | 加入足量饱和Na2CO3溶液,振荡,静置,分液,取出上层液体 |
| A. | A | B. | B | C. | C | D. | D |
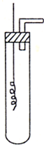 某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.供选择的药品:铜丝、稀硝酸、烧碱溶液、铁粉、CaCO3颗粒.
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.供选择的药品:铜丝、稀硝酸、烧碱溶液、铁粉、CaCO3颗粒.