题目内容
13.如图是由4个碳原子结合成的4种有机物(氢原子没有画出)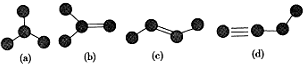
(1)写出有机物(a)的系统命名法的名称2-甲基丙烷.
(2)鉴别有机物(a)和(b)所需要的试剂是溴水或酸性高锰酸钾溶液.
(3)上述有机物中与(c)互为同分异构体的是(b)(填代号).
(4)上述有机物中4个碳原子处于同一平面的有(b)(c)(d)(填代号).
分析 由图可知,(a)为CH(CH3)3,(b)为CH2=C(CH3)2,(c)为CH3CH=CHCH3,(d)为HC≡CCH2CH3.(b)中含有碳碳双键,(a)为烷烃,可以用溴水或酸性高锰酸钾溶液进行区别.(b)与(c)分子式相同,结构不同,二者互为同分异构体.(b)、(c)中存在碳碳双键,不饱和碳原子及其连接的原子处于同一平面,(d)中选择碳碳单键可以使甲基中碳原子处于碳碳双键的平面结构.
解答 解:由图可知,(a)为CH(CH3)3,(b)为CH2=C(CH3)2,(c)为CH3CH=CHCH3,(d)为HC≡CCH2CH3.
(1)有机物(a)的系统命名法的名称:2-甲基丙烷,故答案为:2-甲基丙烷;
(2)(b)中含有碳碳双键,能与溴水发生加成反应,使溴水褪色,能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液褪色,而(a)为烷烃,不能与溴水、酸性高锰酸钾溶液反应,可以用溴水或酸性高锰酸钾溶液进行区别,
故答案为:溴水或酸性高锰酸钾溶液;
(3)(b)与(c)分子式相同,结构不同,二者互为同分异构体,
故答案为:(b);
(4)(a)中3个甲基与H原子连接同一碳原子上,为四面体结构,4个碳原子不可能处于同一平面内,(b)、(c)中存在碳碳双键,不饱和碳原子及其连接的原子处于同一平面,4个碳原子处于同一平面内,(d)中选择碳碳单键可以使甲基中碳原子处于碳碳双键的平面结构,4个碳原子可能处于同一平面内,
故答案为:(b)(c)(d).
点评 本题考查有机物的结构、有机物命名、同分异构体、有机物鉴别等,注意对基础知识的理解掌握,注意根据苯与乙烯的平面结构、乙炔的直线型、甲烷的四面体结构判断分子共面与共线问题.

练习册系列答案
相关题目
3.某研究性学习小组为研究影响化学反应速率的因素,设计如下方案:
已知:反应的方程式(未配平):KMnO4+H2C2O4+H2SO4-K2SO4+CO2↑+H2O.
(1)实验记时方法是从溶液混合开始记时,至紫红色刚好褪去时记时结束.
(2)实验Ⅰ和Ⅱ研究浓度对反应速率的影响,实验Ⅰ和Ⅲ研究温度对反应速率的影响.请在上表空格中填入合理的实验数据.
(3)从实验数据分析,实验Ⅰ和Ⅳ研究催化剂对反应的影响.
(4)利用反应6NO2+8NH3═7N2+12H2O构成原电池,能消除氮氧化物的排放,减轻环境污染,装置如图所示.
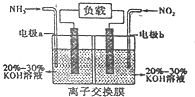
①电极a为负极,其电极反应式为2NH3-6e-+60H-=N2+6H2O.
②当有2.24L NO2(标准状况下)被处理时,转移电子为0.4mol.
③为使电池持续放电,该离子交换膜需选用阴离子交换膜.
| 实验编号 | 0.01mol•L-1酸性KMnO4溶液 | 0.1mol•L-1H2C2O4溶液 | 水 | 1mol•L-1MnSO4溶液 | 反应温度/℃ | 反应时间 |
| Ⅰ | 2mL | 2mL | 0 | 0 | 20 | 125 |
| Ⅱ | 2mL | 1mL | 1mL | 0 | 20 | 320 |
| Ⅲ | 2mL | 2mL | mL | 0 | 50 | 30 |
| Ⅳ | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
(1)实验记时方法是从溶液混合开始记时,至紫红色刚好褪去时记时结束.
(2)实验Ⅰ和Ⅱ研究浓度对反应速率的影响,实验Ⅰ和Ⅲ研究温度对反应速率的影响.请在上表空格中填入合理的实验数据.
(3)从实验数据分析,实验Ⅰ和Ⅳ研究催化剂对反应的影响.
(4)利用反应6NO2+8NH3═7N2+12H2O构成原电池,能消除氮氧化物的排放,减轻环境污染,装置如图所示.

①电极a为负极,其电极反应式为2NH3-6e-+60H-=N2+6H2O.
②当有2.24L NO2(标准状况下)被处理时,转移电子为0.4mol.
③为使电池持续放电,该离子交换膜需选用阴离子交换膜.
4.下表列出了2种燃煤烟气脱硫方法的原理:
(1)方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O═(NH4)2SO3;4NH3+2SO2+2H2O+O2═2(NH4)2SO4.下列说法正确的是AC(填字母).
A.两个都是化合反应
B.两个都是氧化还原反应
C.可以用HCl鉴别(NH4)2SO3、(NH4)2SO4溶液
D.可以用Ba(OH)2鉴别(NH4)2SO3、(NH4)2SO4两种溶液
(2)方法Ⅱ中发生的化学反应方程式为SO2+CaO=CaSO3、2CaSO3+O2=2CaSO4.
(3)①某地化石燃料煤的使用量很大,收集该地区的雨水,经测pH5.6,放置一个星期后,再测pH应小于5.6(填“大于”、“小于”或“等于”),原因是2H2SO3+O2=2H2SO4(用化学方程式表示).
②为了变废为宝,该地将SO2炉气精制获得精制炉气,将精制炉气(含SO2、O2、N2)催化氧化以便制取硫酸.在实际生产中,此反应可选择的反应条件:A.常压、450℃左右,SO2转化率为95% B.10个大气压、450℃左右,SO2转化率为97.5%应选择A(填“A”或“B”).
| 方法Ⅰ | 用氨水将SO2转化为(NH4)2SO3、(NH4)2SO4 |
| 方法Ⅱ | 用生石灰吸收SO2,再转化为CaSO4 |
A.两个都是化合反应
B.两个都是氧化还原反应
C.可以用HCl鉴别(NH4)2SO3、(NH4)2SO4溶液
D.可以用Ba(OH)2鉴别(NH4)2SO3、(NH4)2SO4两种溶液
(2)方法Ⅱ中发生的化学反应方程式为SO2+CaO=CaSO3、2CaSO3+O2=2CaSO4.
(3)①某地化石燃料煤的使用量很大,收集该地区的雨水,经测pH5.6,放置一个星期后,再测pH应小于5.6(填“大于”、“小于”或“等于”),原因是2H2SO3+O2=2H2SO4(用化学方程式表示).
②为了变废为宝,该地将SO2炉气精制获得精制炉气,将精制炉气(含SO2、O2、N2)催化氧化以便制取硫酸.在实际生产中,此反应可选择的反应条件:A.常压、450℃左右,SO2转化率为95% B.10个大气压、450℃左右,SO2转化率为97.5%应选择A(填“A”或“B”).
1.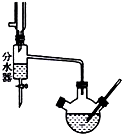 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表
请回答有关问题.
Ⅰ.乙酸正丁酯粗产品的制备在三孔圆底烧瓶中进行,并使用了分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管.实验需要的药品:浓硫酸、冰醋酸和正丁醇.
(1)写出生成乙酸正丁酯的方程式CH3CH2CH2CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3CH2CH2CH2OOCCH3+H2O.
(2)正丁醇的核磁共振氢谱中峰面积之比是3:2:2:2:1.
(3)结合平衡移动原理进一步解释分水器的作用分离出生成的水,使得平衡向生成乙酸正丁酯的方向移动.
Ⅱ.乙酸正丁酯粗产品的精制
(1)将三颈圆底烧瓶中的液体转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是先放出下层的水层,再将有机层从上口倒入一个干燥的蒸馏烧瓶中.
(2)将酯层进行蒸馏.收集乙酸正丁酯产品.
Ⅲ.计算产率
如果实验中加入了18.5mL正丁醇、30mL冰醋酸和2mL浓硫酸,实验后制得的乙酸正丁酯的质量为0.11mol,则乙酸正丁酯的产率为55%.
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
Ⅰ.乙酸正丁酯粗产品的制备在三孔圆底烧瓶中进行,并使用了分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管.实验需要的药品:浓硫酸、冰醋酸和正丁醇.
(1)写出生成乙酸正丁酯的方程式CH3CH2CH2CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3CH2CH2CH2OOCCH3+H2O.
(2)正丁醇的核磁共振氢谱中峰面积之比是3:2:2:2:1.
(3)结合平衡移动原理进一步解释分水器的作用分离出生成的水,使得平衡向生成乙酸正丁酯的方向移动.
Ⅱ.乙酸正丁酯粗产品的精制
(1)将三颈圆底烧瓶中的液体转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是先放出下层的水层,再将有机层从上口倒入一个干燥的蒸馏烧瓶中.
(2)将酯层进行蒸馏.收集乙酸正丁酯产品.
Ⅲ.计算产率
如果实验中加入了18.5mL正丁醇、30mL冰醋酸和2mL浓硫酸,实验后制得的乙酸正丁酯的质量为0.11mol,则乙酸正丁酯的产率为55%.
8.下面有四种有机物,用提供的试剂分别鉴别,将所用试剂及产生的现象的序号填在相应横线上.
①cB②bC③dA④aD
①cB②bC③dA④aD
| 有机物 | 试剂 | 现象 |
| ①淀粉 ②苯乙烯 ③苯酚 ④蛋白质 | a.浓硝酸 b.酸性高锰酸钾溶液 c.碘水 d.FeCl3溶液 | A.呈紫色 B.呈蓝色 C.紫色褪去 D.呈黄色 |
18.下列物质中不属于天然高分子化合物的是( )
| A. | 纤维素 | B. | 蛋白质 | C. | 油脂 | D. | 淀粉 |
5.我国正在推广使用乙醇汽油;所谓乙醇汽油就是在汽油中加入适量乙醇(一般为10:1)混合而成的一种燃料.下列有关的叙述错误的是( )
| A. | 由石油可以制得汽油 | |
| B. | 乙醇汽油是一种新型的化合物 | |
| C. | 汽车使用乙醇汽油可以减少有害气体的排放 | |
| D. | 由玉米、高梁发酵可以制得乙醇 |
2.物质在下列应用中,利用了其还原性的是( )
| A. | 纯碱去油污 | B. | 铝冶炼金属 | C. | 硝酸制炸药 | D. | 漂粉精漂白织物 |
3.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 物质的量浓度为1mol/L的K2SO4溶液中,含2mol K+ | |
| B. | 把40g NaOH固体溶于水得到1 L溶液,所得溶液中NaOH的物质的量浓度为1mol•L-1 | |
| C. | 常温常压下,71 g Cl2含有2 NA个Cl原子 | |
| D. | 标准状况下,11.2 L N2中含有的电子数为7NA |