题目内容
16.镁/H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是( )| A. | 电池总反应的离子方程式为:Mg+H2O2+2H+═Mg2++2H2O | |
| B. | 负极的电极反应为:H2O2+2H++2e-═2H2O | |
| C. | 工作时,正极周围海水的pH减小 | |
| D. | 电池工作时,溶液中的H+向负极移动 |
分析 镁-H2O2酸性燃料电池中,镁为活泼金属,应为原电池的负极,被氧化,电极反应式为Mg-2e-═Mg2+,H2O2具有氧化性,应为原电池的正极,被还原,电极反应式为H2O2+2H++2e-═2H2O,根据电极反应式判断原电池总反应式,根据电极反应判断溶液PH的变化.
解答 解:A、电解质溶液呈酸性,不可能生成Mg(OH)2,电池总反应应为Mg+H2O2+2H+═Mg2++2H2O,故A正确;
B、镁为活泼金属,应为原电池的负极,被氧化,电极反应式为Mg-2e-═Mg2+,故B错误;
C、工作时,正极反应式为H2O2+2H++2e-═2H2O,不断消耗H+离子,正极周围海水的pH增大,故C错误;
D、原电池中,阳离子向正极移动,阴离子向负极移动,形成闭合回路,所以溶液中的H+向正极移动,故D错误.
故选A.
点评 本题考查原电池知识,题目难度中等,注意电极反应式的书写和电解质溶液的酸碱性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO?2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下,用气体传感器测得不同时间的NO和CO浓度如下表:
请回答:(以下各题均不考虑温度变化对催化效率的影响):
(1)前2s内的平均反应速度v (N2)=1.875×10-4mol•L-1•s-1;
(2)在该温度下,反应的平衡常数K=5000,若升高温度时,K值变小,则该反应的△H<0 (填写“>”、“<”、“=”);
(3)若在容器中发生上述反应,达平衡后,下列措施能提高NO转化率的是CD
A.加入催化剂 B.升高温度 C.降低温度D.缩小容器体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组对比实验,部分实验条件已经填在下面实验设计表中,请在下面设计表的空格中填入剩余的实验条件数据.
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)前2s内的平均反应速度v (N2)=1.875×10-4mol•L-1•s-1;
(2)在该温度下,反应的平衡常数K=5000,若升高温度时,K值变小,则该反应的△H<0 (填写“>”、“<”、“=”);
(3)若在容器中发生上述反应,达平衡后,下列措施能提高NO转化率的是CD
A.加入催化剂 B.升高温度 C.降低温度D.缩小容器体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组对比实验,部分实验条件已经填在下面实验设计表中,请在下面设计表的空格中填入剩余的实验条件数据.
| 实验编号 | T/℃ | NO初始浓度 ( mol•L-1) | CO初始浓度 ( mol•L-1) | 催化剂的比表面积 ( m2•g-1) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
4.在一定温度时,将1mol A和2mol B放入容积为5L 的某密闭容器中发生如下反应:A(s)+2B(g)?C(g)+2D(g),经5min后,测得容器内B的浓度减少了0.2mol•L-1.下列叙述不正确的是( )
| A. | 5min时容器内气体总的物质的量为3mol | |
| B. | 5min时,容器内D的浓度为0.2mol•L-1 | |
| C. | 该可逆反应随反应的进行,容器内压强逐渐增大 | |
| D. | 在5min内该反应用C的浓度变化表示的反应速率为0.02mol•L-1•min-1 |
11.下列各项操作中不发生先沉淀后溶解现象的是( )
①向饱和Na2CO3溶液中通入过量CO2
②向Fe(OH)3胶体中逐滴滴入过量的H2SO4
③向Ba(NO3)2溶液中通入过量SO2
④向石灰水中通入过量CO2
⑤向Na2SiO3溶液中滴入过量的盐酸.
①向饱和Na2CO3溶液中通入过量CO2
②向Fe(OH)3胶体中逐滴滴入过量的H2SO4
③向Ba(NO3)2溶液中通入过量SO2
④向石灰水中通入过量CO2
⑤向Na2SiO3溶液中滴入过量的盐酸.
| A. | ①③⑤ | B. | ①②⑤ | C. | ①②③⑤ | D. | ①②③ |
5.向X的溶液中加入Y试剂,产生沉淀的量变化关系符合下图所示的情形的是( )
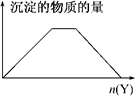

| A. | 向NaOH和Ca(OH)2的混合溶液中通入CO2 | |
| B. | 向HCl和AlCl3的混合溶液中滴加溶液 | |
| C. | 向KAl(SO4)2溶液中滴加NaOH溶液 | |
| D. | 向NH4Cl和MgCl2的混合溶液中滴加NaOH溶液 |
 砷化镓属于第三代半导体,其晶胞结构如如图所示.请回答下列问题:
砷化镓属于第三代半导体,其晶胞结构如如图所示.请回答下列问题: