题目内容
5.向X的溶液中加入Y试剂,产生沉淀的量变化关系符合下图所示的情形的是( )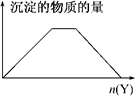
| A. | 向NaOH和Ca(OH)2的混合溶液中通入CO2 | |
| B. | 向HCl和AlCl3的混合溶液中滴加溶液 | |
| C. | 向KAl(SO4)2溶液中滴加NaOH溶液 | |
| D. | 向NH4Cl和MgCl2的混合溶液中滴加NaOH溶液 |
分析 图中关系体现的是沉淀的量随着Y的物质的量的加入,开始逐渐增大,然后保持不变,然后再溶解,且沉淀生成和溶解时消耗的Y的量相等,结合所给物质的性质及相互反应解答.
解答 解:A.向NaOH和Ca(OH)2的混合溶液中通入CO2,二氧化碳先与氢氧化钙反应生成碳酸钙沉淀,发生反应为:Ca(OH)2+CO2═CaCO3↓+H2O,然后在与氢氧化钠反应生成碳酸氢钠,沉淀的量不变,最后发生反应:CaCO3↓+H2O+CO2═Ca(HCO3)2,沉淀溶解,且生成沉淀和沉淀溶解消耗的CO2相等,图象与反应符合,故A正确;
B.向HCl和AlCl3的混合溶液中滴加氢氧化钠溶液,氢氧化钠先与盐酸反应,此段不会产生沉淀,所以开始无沉淀,盐酸消耗后,氢氧化钠再与氯化铝反应先生成氢氧化铝,然后氢氧化铝再溶解,所以与图象不符合,故B错误;
C.向KAl(SO4)2溶液中滴加NaOH溶液,先发生反应铝离子与氢氧根离子生成氢氧化铝沉淀,离子方程式:Al3++3OH-═Al(OH)3↓,然后再发生氢氧化铝与氢氧化钠的反应:Al(OH)3+OH-═AlO2-+2H2O,沉淀铝离子用的氢氧化钠与溶解氢氧化铝用的氢氧化钠的物质的量之比为3:1,且不会出现沉淀保持不变的过程,所以与图象不符合,故C错误;
D.向NH4Cl和MgCl2的混合溶液中滴加NaOH,先发生Mg2++2OH-═Mg(OH)2↓,再发生NH4++OH-═NH3.H2O,先产生沉淀,后沉淀不会溶解,图象与发生的化学反应不符,故D错误;
故选:A.
点评 本题考查了化学反应与图象关系,明确图象表达的含义及离子反应的先后顺序是解题关键,注意反应为用量对反应的影响,题目难度中等.

练习册系列答案
相关题目
16.镁/H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是( )
| A. | 电池总反应的离子方程式为:Mg+H2O2+2H+═Mg2++2H2O | |
| B. | 负极的电极反应为:H2O2+2H++2e-═2H2O | |
| C. | 工作时,正极周围海水的pH减小 | |
| D. | 电池工作时,溶液中的H+向负极移动 |
13.2007年10月24日18时05 分,就在这天与山、山与水的环拥之中,“嫦娥奔月”,一个流传了千年的神话,中国首颗探月卫星发射,在有着“月亮城”之称的高原航天城梦想成真.发射嫦娥一号卫星的长征三号甲运载火箭的第三级发动机使用的低温燃料为液氧和液氢.下列有关说法不正确的是( )
| A. | 液氧和液氢最好在临发射前的一段时间加注 | |
| B. | 氢气可由电解水获得 | |
| C. | 燃烧产物对发射环境没有污染 | |
| D. | 氢是一次能源,可以自己产生 |
20.乙烯是农业上常用的一种催熟剂,能够促进果实的成熟,下列关于有关说不正确的是( )
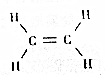
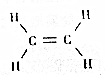
| A. | 乙烯是由碳、氢两种元素组成的 | |
| B. | 乙烯中碳元素的质量分数为85.7% | |
| C. | 乙烯是一种有机高分子化合物 | |
| D. | 乙烯中碳、氢两种元素的原子个数比是1:2 |
16.甲乙丙是三种不含相同离子的可溶性电解质.他们所含的离子如右表所示.取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)<c(乙)<c(丙),下列说法正确的是( )
| 阳离子 | Na+NH4+Fe3+ |
| 阴离子 | OH- Cl- SO42- |
| A. | 甲中一定含有Na+ | B. | 乙中一定含有NH4+ | ||
| C. | 丙中一定含有 Fe3+ | D. | 丙中一定含有SO42- |