题目内容
19.在KNO3、MgSO4、K2SO4组成的混合溶液中Mg2+0.5mol、NO3-0.2mol、SO42-0.6mol,则溶液中K+的物质的量为( )| A. | 0.4mol | B. | 0.3mol | C. | 0.2mol | D. | 0.1mol |
分析 溶液遵循电荷守恒,则阳离子的电荷总数等于阴离子的电荷总数,以此来解答.
解答 解:混合溶液中Mg2+0.5mol、NO3-0.2mol、SO42-0.6mol,设液中K+的物质的量为x,
由电荷守恒可知,x+0.5×2=0.2+0.6×2,解得x=0.4mol,
故选A.
点评 本题考查物质的量的计算,为高频考点,把握电荷守恒为解答的关键,侧重分析与计算能力的考查,注意离子的电荷数计算,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.某有机物是一种医药中间体.其结构简式如图所示.下列有关该物质的说法正确的是( )
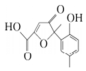

| A. | 该化合物分子中不含手性碳原子 | |
| B. | 该化合物与NaHCO3溶液作用有CO2气体放出 | |
| C. | 1 mol该化合物与足量溴水反应,消耗2 mol Br2 | |
| D. | 在一定条件下,该化合物与HCHO能发生缩聚反应 |
19.下列有关物质的性质与用途具有对应关系的是( )
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | 碳酸氢钠能与碱反应,可用作食品的膨松剂 | |
| C. | 四氯化碳密度比水大,可用于萃取溴水中的Br2 | |
| D. | MgO、Al2O3的熔点都很高,都可用作耐火材料 |
7.科技工作者制造出厚度只有l微米的超薄太阳能电池.硅太阳能电池工作原理如图所示:

下列有关判断错误的是( )

下列有关判断错误的是( )
| A. | 硅原子最外层有4个电子 | |
| B. | 太阳能电池是一种化学电源 | |
| C. | 太阳能电池实现了光能向电能的转化 | |
| D. | B电极为电源正极 |
14.室温下,下列溶液等体积混合后pH一定大于7的是( )
| A. | pH=3的醋酸与pH=11的氢氧化钾 | B. | 0.1mol/L的盐酸与0.1mol/L的氨水 | ||
| C. | 0.001mol/L的盐酸与pH=11的氨水 | D. | pH=3的盐酸与0.001mol/L的氨水 |
4.下列表示正确的是( )
| A. | -CH3(甲基)的电子式为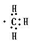 | B. | 乙烯分子的结构简式:CH2CH2 | ||
| C. | H2O分子的球棍模型: | D. | 氟的原子结构示意图: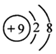 |
8.下列物质按照单质、氧化物、混合物的顺序排列的是( )
| A. | 铁、氧化铁、氯化铁 | B. | 冰、干冰、可燃冰 | ||
| C. | 氧气、二氧化碳、空气 | D. | 金刚石、铁矿石、石灰石 |
9.在体积固定的密闭容器中,发生反应2CO(g)+4H2(g)?CH3CH2OH(g)+H2O(g).下列叙述说明该反应已达到化学平衡状态的是( )
| A. | 混合气体密度不变 | |
| B. | 体系压强不变 | |
| C. | 混合气体的平均相对分子质量不变 | |
| D. | 反应体系中乙醇的物质的量浓度不再变化 |
 某科研单位利用电化学原理用SO2来制备硫酸,装置如图,含有某种催
某科研单位利用电化学原理用SO2来制备硫酸,装置如图,含有某种催