��Ŀ����
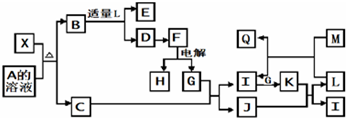
X��һ�����������ϣ�����̼���裨SiC���ṹ���ơ�������������� X�����µ�ת����ϵ�����У�C��һ����ʹʪ��ĺ�ɫʯ����ֽ��������ɫ���壬DΪ��ɫ��״������E��Һ����ɫ��Ӧ����ʻ�ɫ��M��һ�ֳ���������������M��L������Q��I��
��1��X��A��Һ��Ӧ�����ӷ���ʽΪ ��
��2���Ѻ��ȵ�ľ̿Ͷ�뵽L��Ũ��Һ�У��ɷ������ҷ�Ӧ��
�ٻ�ѧ����ʽΪ ��
�����Ѳ���������ͨ�������ı���̼��������Һ�У��ٰ��ݳ�����������ͨ�������Ĺ������ƹ��壬��ַ�Ӧ����ͨ��ˮ�У�����ռ����������� ��
�����Ѳ���������ֱ��ͨ�������ij���ʯ��ˮ�У������� ��
��3����K��I��G��������������������ˮ���У�������ȫ�ܽ⣬��Һ�������������������ߵ����ʵ���֮�ȿ���Ϊ ��
A��1��1��1 B��4��2��2.5 C��4��8��7 D��6��4��5��

��1��X��A��Һ��Ӧ�����ӷ���ʽΪ
��2���Ѻ��ȵ�ľ̿Ͷ�뵽L��Ũ��Һ�У��ɷ������ҷ�Ӧ��
�ٻ�ѧ����ʽΪ
�����Ѳ���������ͨ�������ı���̼��������Һ�У��ٰ��ݳ�����������ͨ�������Ĺ������ƹ��壬��ַ�Ӧ����ͨ��ˮ�У�����ռ�����������
�����Ѳ���������ֱ��ͨ�������ij���ʯ��ˮ�У�������
��3����K��I��G��������������������ˮ���У�������ȫ�ܽ⣬��Һ�������������������ߵ����ʵ���֮�ȿ���Ϊ
A��1��1��1 B��4��2��2.5 C��4��8��7 D��6��4��5��
���㣺������ƶ�
ר�⣺�ƶ���
������C��һ����ʹʪ��ĺ�ɫʯ����ֽ��������ɫ����ΪNH3��DΪ��ɫ��״����������ɵ�F����ж�DΪAl��OH��3��FΪAl2O3��GΪO2��HΪAl���Ѻ��ȵ�ľ̿Ͷ�뵽L��Ũ��Һ�У��ɷ������ҷ�Ӧ�������ж�IΪNO��JΪH2O��KΪNO2��LΪHNO3��M��һ�ֳ���������������M��L������Q��I��֤��MΪFe��QΪFe��NO3��2��ת����ϵ�У�E��Һ����ɫ��Ӧ����ʻ�ɫ˵������Ԫ�أ�B�����������ᷴӦ������������������E��֤��BΪƫ������NaAlO2��EΪNaNO3��X��һ�����������ϣ�����̼���裨SiC���ṹ���ơ����������������Ϻ�A��Ӧ�����ж�XΪAlN��AΪ����������Һ����϶�Ӧ���ʵ������Լ���ĿҪ��ɽ����⣮
���
�⣺C��һ����ʹʪ��ĺ�ɫʯ����ֽ��������ɫ����ΪNH3��DΪ��ɫ��״����������ɵ�F����ж�DΪAl��OH��3��FΪAl2O3��GΪO2��HΪAl���Ѻ��ȵ�ľ̿Ͷ�뵽L��Ũ��Һ�У��ɷ������ҷ�Ӧ�������ж�IΪNO��JΪH2O��KΪNO2��LΪHNO3��M��һ�ֳ���������������M��L������Q��I��֤��MΪFe��QΪFe��NO3��2��ת����ϵ�У�E��Һ����ɫ��Ӧ����ʻ�ɫ˵������Ԫ�أ�B�����������ᷴӦ������������������E��֤��BΪƫ������NaAlO2��EΪNaNO3��X��һ�����������ϣ�����̼���裨SiC���ṹ���ơ����������������Ϻ�A��Ӧ�����ж�XΪAlN��AΪ����������Һ��
��1��X��A��Һ��Ӧ�����ӷ���ʽΪ��AlN+H2O+OH-=AlO2-+NH3�����ʴ�Ϊ��AlN+H2O+OH-=AlO2-+NH3����
��2���Ѻ��ȵ�ľ̿Ͷ�뵽L��HNO3����Ũ��Һ�У��ɷ������ҷ�Ӧ��
�ٻ�ѧ����ʽΪ��C+4HNO3��Ũ��
CO2��+4NO2��+2H2O���ʴ�Ϊ��C+4HNO3��Ũ��
CO2��+4NO2��+2H2O��
�ڰѲ���������ͨ�������ı���̼��������Һ�У����ն�����̼�Ͷ����������ʵ���Ϊ1��4��������Ӧ3NO2+H2O=2HNO3+NO���õ�������̼1+
=
��һ������
���ٰ��ݳ�����������ͨ�������Ĺ������ƹ��壬��ַ�Ӧ����������
����ͨ��ˮ�У����ݷ�Ӧ���㣺4NO+O2+2H2O=4HNO3��һ������ȫ����Ӧ��ʣ������=
-
=
=1.5������ռ���������ΪO2��
�ʴ�Ϊ��O2��
�۰Ѳ���������ֱ��ͨ�������ij���ʯ��ˮ�У�����������ˮ��Ӧ���������һ��������������������Ʒ�Ӧ�����Կ�ʼ����������а�ɫ����̼������ɣ�һ���������������е�������Ӧ���ɶ����������壬��Һ�Ϸ����ֺ���ɫ��
�ʴ�Ϊ����ʼ����������а�ɫ�������ɣ���Һ�Ϸ����ֺ���ɫ��
��3����K��NO2����I��NO����G��O2����������������������ˮ���У�������ȫ�ܽ⣬��Һ�������������������ߵ����ʵ���֮�ȿ���Ϊ��
A��1��1��1ʱ��NO2+NO+O2+H2O=2HNO3���������ȫ���ܽ⣬��A���ϣ�
B��4��2��2.5 ʱ������4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O=4HNO3����������ǡ������ˮ����B���ϣ�
C��4��8��7������4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O=4HNO3����������ǡ������ˮ����C���ϣ�
D��6��4��5������4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O=4HNO3���������㷴Ӧ��ʣ������0.5�����岻��ȫ������ˮ����D�����ϣ�
�ʴ�Ϊ��ABC��
��1��X��A��Һ��Ӧ�����ӷ���ʽΪ��AlN+H2O+OH-=AlO2-+NH3�����ʴ�Ϊ��AlN+H2O+OH-=AlO2-+NH3����
��2���Ѻ��ȵ�ľ̿Ͷ�뵽L��HNO3����Ũ��Һ�У��ɷ������ҷ�Ӧ��
�ٻ�ѧ����ʽΪ��C+4HNO3��Ũ��
| ||
| ||
�ڰѲ���������ͨ�������ı���̼��������Һ�У����ն�����̼�Ͷ����������ʵ���Ϊ1��4��������Ӧ3NO2+H2O=2HNO3+NO���õ�������̼1+
| 8 |
| 3 |
| 11 |
| 3 |
| 4 |
| 3 |
| 11 |
| 6 |
| 11 |
| 6 |
| 1 |
| 3 |
| 9 |
| 6 |
�ʴ�Ϊ��O2��
�۰Ѳ���������ֱ��ͨ�������ij���ʯ��ˮ�У�����������ˮ��Ӧ���������һ��������������������Ʒ�Ӧ�����Կ�ʼ����������а�ɫ����̼������ɣ�һ���������������е�������Ӧ���ɶ����������壬��Һ�Ϸ����ֺ���ɫ��
�ʴ�Ϊ����ʼ����������а�ɫ�������ɣ���Һ�Ϸ����ֺ���ɫ��
��3����K��NO2����I��NO����G��O2����������������������ˮ���У�������ȫ�ܽ⣬��Һ�������������������ߵ����ʵ���֮�ȿ���Ϊ��
A��1��1��1ʱ��NO2+NO+O2+H2O=2HNO3���������ȫ���ܽ⣬��A���ϣ�
B��4��2��2.5 ʱ������4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O=4HNO3����������ǡ������ˮ����B���ϣ�
C��4��8��7������4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O=4HNO3����������ǡ������ˮ����C���ϣ�
D��6��4��5������4NO2+O2+2H2O=4HNO3��4NO+3O2+2H2O=4HNO3���������㷴Ӧ��ʣ������0.5�����岻��ȫ������ˮ����D�����ϣ�
�ʴ�Ϊ��ABC��
���������⿼��������ƶϣ�Ϊ��Ƶ���㣬�������������ʵ��ۺ�Ӧ�ã���Ҫ���鵪�������Ͳ��ϵ�����Ӧ�ã�������̼�������仯����������ᣬ�������������ʵ�Ӧ�ã���������Ļ�ϼ���Ӧ�ã���Ŀ�ۺ��Դ��ѶȽϴ�

��ϰ��ϵ�д�
 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
�����Ŀ
���и��������У�����ˮ��Һ�д���������ǣ�������
A��Na+��Ca2+��OH-��HCO
| ||
| B��Ca2+��Al3+��NO3-��OH- | ||
C��H+��Mg2+��SO42-��HCO
| ||
| D��Fe2+��Al3+��SO42-��Cl- |
����˵������ȷ���ǣ�������
| A��PCl3�����������Σ�������ΪPԭ������sp3�ӻ��Ľ�� |
| B��������ԭ�Ӳ�ȡsp3�ӻ��ķ��ӣ��伸�ι��Ͷ����������� |
| C��sp3�ӻ�������������1��s�����3��p�������γɵ��ĸ�sp3�ӻ���� |
| D��AB3�͵ķ��ӿռ乹�ͱ�Ϊƽ�������� |
���й��������˵���в���ȷ���ǣ�������
| A�������Ǿ���ǿ�Ҵ̼�����ζ��Һ�� |
| B������ķ��ӿ��Կ����Ǽ����Ȼ��γɵ��л��� |
| C����ˮ�����ֳƱ����ᣬ���Ǵ����� |
| D�����������ˮ���Ҵ� |

 ����ȼ������Һ̬ˮ���Ȼ�ѧ����ʽ��2H2��g��+O2��g���T2H2O��l����
����ȼ������Һ̬ˮ���Ȼ�ѧ����ʽ��2H2��g��+O2��g���T2H2O��l����