题目内容
1.下列操作正确的是( )| A. | 锥形瓶在装待测液前要用待测液润洗2~3次 | |
| B. | 用25mL酸式滴定管量取20.00mLKMnO4溶液 | |
| C. | 测某溶液pH:用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测 | |
| D. | 加热蒸发NaHCO3溶液得纯净的NaHCO3 |
分析 A.滴定时,锥形瓶不能润洗,否则会导致待测液物质的量偏大,测定结果偏高;
B.酸式滴定管下端为玻璃旋塞,可以用于量取一定体积的高锰酸钾溶液;
C.pH试纸测定pH值时,试纸在使用前不能湿润;
D.碳酸氢钠不稳定,受热分解;
解答 解:A.中和滴定时,不能用待测液润洗待测液,否则会导致消耗的标准液体积偏大,沉淀结果偏高,故A错误;
B.碱式滴定管下端为橡胶塞,不能量取具有强氧化性的高锰酸钾溶液,可以用酸式滴定管量取高锰酸钾溶液,故B正确;
C.pH试纸测定pH值时,试纸在使用前不能湿润,容易将溶液稀释测量结果误差较大,故C错误;
D.碳酸氢钠不稳定,受热分解,加热蒸发NaHCO3溶液得到固体为碳酸钠,故D错误;
故选:B.
点评 本题考查了计量仪器的使用方法、pH试纸的使用,掌握常见计量仪器的构造及使用方法,明确pH试纸在使用前不能湿润是解题关键,题目难度不大.

练习册系列答案
相关题目
16.NO2可电解制备绿色硝化试剂N2O5,其原理如图所示,下列说法错误的是( )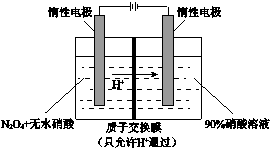

| A. | 阳极电解液中的N2O4可由NO2降温转化制得 | |
| B. | 阳极的电极反应为:N2O4-2e-+2HNO3=2N2O5+2H+ | |
| C. | 阴极的电极反应为:2H++2e-=H2↑ | |
| D. | 每制备1molN2O5,有1molH+通过质子交换膜 |
9.某气态烃1mol跟2mol氯化氢加成,其加成产物又可被8mol氯气完全取代,该烃可能是( )
| A. | 丙烯 | B. | 1-丁烯 | C. | 丙炔 | D. | 2-丁炔 |
16.下列离子方程式正确的是( )
| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 金属钾与水反应:2K+2H2O═2K++2OH-+H2↑ | |
| C. | 铁与稀硝酸反应:Fe+2H+=Fe2++H2↑ | |
| D. | 小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O |
13.取某气态烷烃的一种二卤代产物21.6g与足量的NaOH溶液共热充分反应后,冷却,再用适量的硝酸酸化,最后加入足量硝酸银溶液,得到沉淀37.6g.则此二卤代物的分子式为( )
| A. | C2H5ClBr | B. | C3H6Cl2 | C. | C4H8Br2 | D. | C3H4I2 |
 ②Cl2
②Cl2 ③CO2
③CO2 ④H2O2
④H2O2 ⑤HClO
⑤HClO ⑥HCN
⑥HCN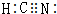
 ⑧Ca(OH)2
⑧Ca(OH)2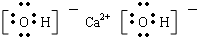 ⑨N2H4
⑨N2H4 ⑩CO(NH2)2
⑩CO(NH2)2 .
.