题目内容
2.20℃时,饱和NaCl溶液的密度为1.12g•cm-3,质量分数是26.5%,则下列说法正确的是( )| A. | 该饱和溶液的物质的量浓度为5.07mol•L-1 | |
| B. | 向该溶液中加入等体积的水之后溶液的质量分数小于13.25% | |
| C. | 25℃时,密度等于1.12g•cm-3的NaCl溶液是饱和溶液 | |
| D. | 将此溶液蒸发掉部分水,再恢复到20℃时,溶液密度一定大于1.12g•cm-3 |
分析 A.物质的量浓度=$\frac{1000ρω}{M}$;
B.水的密度小于饱和氯化钠溶液的密度,则等体积的水质量小于饱和氯化钠溶液的质量;
C.NaCl的溶解度随着温度的升高而增大,当温度升高时,饱和氯化钠溶液的溶解度增大;
D.温度相同时,饱和氯化钠溶液的浓度不变.
解答 解:A.物质的量浓度=$\frac{1000ρω}{M}$=$\frac{1000×1.12×26.5%}{58.5}$mol/L=5.07mol/L,故A正确;
B.水的密度小于饱和氯化钠溶液的密度,则等体积的水质量小于饱和氯化钠溶液的质量,所以向该溶液中加入等体积的水之后溶液的质量分数大于13.25%,故B错误;
C.NaCl的溶解度随着温度的升高而增大,当温度升高时,饱和氯化钠溶液的溶解度增大,所以25℃时,密度等于1.12g•cm-3的NaCl溶液不是饱和溶液,故C错误;
D.温度相同时,饱和氯化钠溶液的浓度不变,将此溶液蒸发掉部分水,再恢复到20℃时,会析出晶体,但溶液浓度不变,则溶液密度一定等于1.12g•cm-3,故D错误;
故选A.
点评 本题考查溶解度及其有关计算,为高频考点,侧重考查学生分析计算能力,明确溶解度含义及其影响因素是解本题关键,易错选项是D,注意:饱和溶液蒸发水分时会析出晶体但浓度不变,题目难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
13.有机物A的结构如图所示,下列说法正确的是( )


| A. | 一定条件下,1 mol A能与3 mol NaOH反应 | |
| B. | 一定条件下,1 mol A能和5 mol氢气发生加成反应 | |
| C. | 一定条件下和浓溴水反应时,1 mol A能消耗3 mol Br2 | |
| D. | A能与碳酸氢钠溶液反应并有气体生成 |
5.以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌.
Ⅰ、制取氯化锌主要工艺如图:
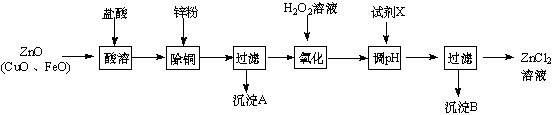
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
(1)加入H2O2溶液发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)流程图中,为了降低溶液的酸度,试剂X可以是abc (选填序号:a.ZnO;b.Zn(OH)2;c.Zn2(OH)2CO3;d.ZnSO4);pH应调整到3.2≤pH<5.2.
(3)氯化锌能催化乳酸(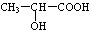 )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为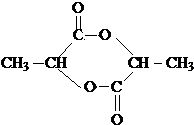 ,聚乳酸的结构简式为
,聚乳酸的结构简式为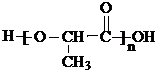 .
.
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)═Na2[Zn(OH)4](aq)},然后电解浸取液.
(4)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
Ⅰ、制取氯化锌主要工艺如图:

已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
(2)流程图中,为了降低溶液的酸度,试剂X可以是abc (选填序号:a.ZnO;b.Zn(OH)2;c.Zn2(OH)2CO3;d.ZnSO4);pH应调整到3.2≤pH<5.2.
(3)氯化锌能催化乳酸(
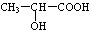 )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为
,聚乳酸的结构简式为 .
.Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)═Na2[Zn(OH)4](aq)},然后电解浸取液.
(4)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
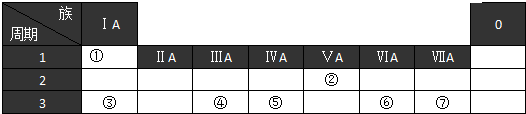
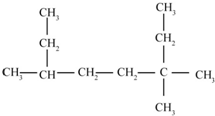 的名称为3,3,6-三甲基辛烷
的名称为3,3,6-三甲基辛烷 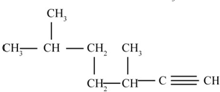 的名称为3,6-二甲基-1-庚炔
的名称为3,6-二甲基-1-庚炔 .
.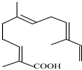 ,其分子式为C15H22O2.
,其分子式为C15H22O2.