题目内容
11.现有下列物质 ①熔化的NaCl ②盐酸 ③石墨 ④纯醋酸 ⑤铜⑥酒精(C2H5OH) ⑦醋酸铵 ⑧液氨 ⑨SO2请用以上物质回答下列问题.(填序号)(1)属于强电解质的是①⑦,且在上述状态下能导电的是①;
(2)属于弱电解质的是④;
(3)属于非电解质,但溶于水后的水溶液能导电的是⑧⑨.
分析 在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液里或熔融状态下都不导电的化合物是非电解质,完全电离的电解质是强电解质,只有部分电离的电解质是弱电解质,能导电的物质中含有自由移动的阴阳离子或自由移动的电子.
解答 解:①熔化的NaCl 属于强电解质,能导电,溶于水导电;
②盐酸是氯化氢的水溶液,是混合物,能导电;
③石墨是单质,既不是电解质也不是非电解质,但能导电;
④纯醋酸属于弱电解质,本身不能导电,其水溶液能导电;
⑤铜是单质,既不是电解质也不是非电解质,但能导电;
⑥酒精(C2H5OH)属于非电解质,但其水溶液不导电;
⑦醋酸铵是盐不能导电,水溶液中能导电,且属于强电解质;
⑧液氨不能导电属于非电解质,溶于水导电;
⑨SO2不能导电属于非电解质,溶于水导电;
(1)属于强电解质的是①⑦,且在上述状态下能导电的是①,
故答案为:①⑦,①;
(2)属于弱电解质的是④,故答案为:④;
(3)属于非电解质,但溶于水后的水溶液能导电的是⑧⑨,
故答案为:⑧⑨;
点评 本题考查了强弱电解质、非电解质的判断,注意电解质不一定导电,导电的不一定是非电解质,为易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列反应达到化学平衡后,加压或升温都能使化学平衡向逆反应方向移动的是( )
| A. | SO2(g)+NO2(g)?SO3(g)+NO(g)△H<0 | B. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 | ||
| C. | C(s)+CO2(g)?2CO(g)△H>0 | D. | H2S(g)?H2(g)+S(s)△H>0 |
2.下列关于反应能量的说法正确的是( )
| A. | A、101kPa时,2H2(g)+O2(g)═2H2O(g)△H=-Q kJ•mol-1,则H2的燃烧热为$\frac{1}{2}$Q kJ•mol-1 | |
| B. | B、同温同压下,H2(g)+Cl2(g)═2HCl(g) 在光照和点燃条件下的△H相同 | |
| C. | C、500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热3kJ,其热化学方程式为N2(g)+3H2(g) $?_{催化剂}^{500℃,30MPa}$2NH3(g)△H=-38.6kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,则含1mol NaOH的氢氧化钠溶液与含0.5mol H2SO4的浓硫酸混合后放出57.3kJ的热量 |
6.下列事实能够说明亚硝酸(HNO2)为弱电解质的是( )
| A. | 亚硝酸不与硫酸钠溶液反应 | |
| B. | PH相等的亚硝酸和硫酸溶液各自稀释10倍体积后,亚硝酸的PH比硫酸的小 | |
| C. | 25℃时,HNO2的水溶液的PH<7 | |
| D. | 用亚硝酸溶液做导电实验时,灯泡很暗 |
3.下列离子方程式或化学方程式与所述事实相符且正确的是( )
| A. | 向0.1 mol/L、pH=1的NaHA溶液中加入NaOH溶液:H++OH-═H2O | |
| B. | 以金属银为阳极电解饱和NaCl溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ H2↑+Cl2↑+2OH- | |
| C. | 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O═3I2+6OH- | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
20.具有漂白性和还原性的无色气体是( )
| A. | Cl2 | B. | NO2 | C. | NH3 | D. | SO2 |
1.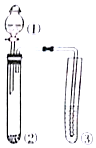 利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )
利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )
 利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )
利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )| 选项 | ① | ② | ③ | 试管③中现象 |
| A | 浓盐酸 | Na2SO3 | Ba(NO3)2溶液 | 无现象 |
| B | 稀盐酸 | 大理石 | 苯酚钠溶液 | 产生白色沉淀 |
| C | 稀盐酸 | 大理石 | CaCl2溶液 | 产生白色沉淀 |
| D | 浓硫酸 | 铜片 | KI-淀粉溶液 | 溶液变蓝 |
| A. | A | B. | B | C. | C | D. | D |

 的名称为3,6-二甲基-1-庚炔.
的名称为3,6-二甲基-1-庚炔.