题目内容
14.有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A的单质和它的一种氧化物是工业生产上常用的还原剂.B的最外层电子数是次外层的3倍;0.1molC的单质能从酸溶液中置换出2.24L标准状况下的氢气;又知B、C、D所形成的简单离子的电子层结构相同,B和E是同主族的元素.请回答下列问题:(1)请依次写出A、C、E三种元素的元素符号:C、Mg、S.
(2)请写出A的最高价氧化物的电子式
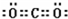 ;E的单质在空气中燃烧所生成物质的化学式SO2.
;E的单质在空气中燃烧所生成物质的化学式SO2.(3)A元素可以形成多种同素异形体,其中硬度最大,不导电的是金刚石(填物质名称);熔点高,可以导电的是石墨(填物质名称).
(4)请写出C的单质与A、B形成的化合物反应的化学方程式2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
分析 有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,B的最外层电子数是次外层的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故B为O元素;B和E是同主族的元素,则E为S元素;A的单质和它的一种氧化物是工业生产上常用的还原剂,则A为碳元素;0.1molC的单质能从酸溶液中置换出2.24L标准状况下的氢气,则C为金属,其化合价=$\frac{\frac{2.24L}{22.4L/mol}×2}{0.1mol}$=+2,故C为Mg;B、C、D所形成的简单离子的电子层结构相同,则离子核外电子数为10,结合原子序数可知D为Al,据此解答.
解答 解:有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,B的最外层电子数是次外层的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故B为O元素;B和E是同主族的元素,则E为S元素;A的单质和它的一种氧化物是工业生产上常用的还原剂,则A为碳元素;0.1molC的单质能从酸溶液中置换出2.24L标准状况下的氢气,则C为金属,其化合价=$\frac{\frac{2.24L}{22.4L/mol}×2}{0.1mol}$=+2,故C为Mg;B、C、D所形成的简单离子的电子层结构相同,则离子核外电子数为10,结合原子序数可知D为Al.
(1)由上述分析可知,A、C、E三种元素的元素符号分别为:C、Mg、S,故答案为:C;Mg;S;
(2)A的最高价氧化物为CO2,分子中碳原子与氧原子之间形成2对共用电子对,其电子式为: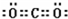 ,S的单质在空气中燃烧所生成二氧化硫,其质的化学式为SO2,
,S的单质在空气中燃烧所生成二氧化硫,其质的化学式为SO2,
故答案为: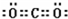 ;SO2;
;SO2;
(3)A元素可以形成多种同素异形体,其中硬度最大,不导电的是金刚石,熔点高,可以导电的是石墨,
故答案为:金刚石;石墨;
(4)C的单质与A、B形成的化合物反应,为Mg在二氧化碳中燃烧生成MgO与碳,化学反应方程式:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
点评 本题考查元素位置结构性质关系及应用,题目难度不大,侧重于元素化合物性质与常用化学用语考查,学习中注意基础知识的全面掌握.

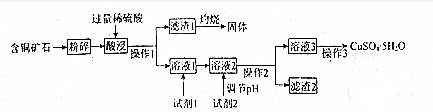
已知:ⅰ.试剂价格:漂液(含25.2%NaClO)450元/吨,双氧水(含30%H2O2)2400元/吨.
ⅱ.溶液中离子浓度小于等于1.0×10-5mol•L-1时,认为该离子沉淀完全.
ⅲ.25℃时,金属离子生成氢氧化物时,开始沉淀和沉淀完全的pH如表所示,
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 4.0 | 6.5 |
(1)含铜矿石粉碎的目的为增大矿石与稀硫酸的接触面积,加快酸浸速率并使酸浸更充分,滤渣Ⅰ灼烧所得固体的用途为制备光导纤维、制备玻璃、生产硅单质等(任写一种).
(2)操作Ⅰ所用的玻璃仪器为烧杯、漏斗、玻璃棒.
(3)试剂1的名称为漂液,选择该试剂的理由为节约成本,所发生反应的离子方程式为ClO-+2Fe2++2H+=Cl-+2Fe3++H2O.
(4)加入试剂2,需调节溶液的pH的合理范围为3.7≤PH<4.0,试剂2可以选择下列物质中的BC(填选项字母).
A.Cu B.CuO C.Cu(OH)2 D.Fe
(5)操作3包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥、洗涤的方法为用玻璃棒引流向过滤器中加入冷水至浸没沉淀,待水自然流下,重复2-3次.
(6)25℃时,Cu(OH)2 的溶度积常数K溶[Cu(OH)2]=1.0×10-20.
| A. | 原子 | B. | 分子 | C. | 核素 | D. | 元素 |
| A. | SO2通入到BaCl2溶液中:Ba2++SO2+H2O=BaSO3↓+2H+ | |
| B. | 浓H2SO4与硫化亚铁制取H2S气体:H2SO4+FeS=Fe2++SO42-+H2S↑ | |
| C. | SO2使溴水褪色:SO2+2H2O+Br2=4H++SO42-+2Br- | |
| D. | 氯化铵固体与熟石灰共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
| A. | 铝的原子失电子能力比镁强 | B. | 氟的氢化物很稳定 | ||
| C. | 水比硫化氢稳定 | D. | 氢氧化钠比氢氧化镁的碱性强 |
| A. | 21% | B. | 25% | C. | 30% | D. | 35% |
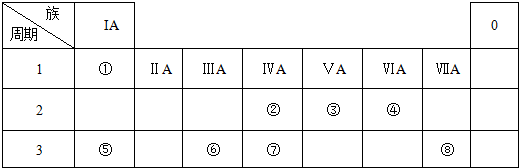
| A. | 元素周期表揭示了化学元素间的内在联系,是化学发展史上重要里程碑 | |
| B. | 在周期表中,把电子层数相同的元素排成一横行,称为一周期 | |
| C. | 元素周期表中,总共有18个纵行,18个族,IIIB族含有32种金属元素 | |
| D. | 第IA族(除H)元素又称为碱金属元素,第ⅦA族元素又称为卤族元素 |
| A. | 非金属性 Z>Y>X | B. | 原子半径 X>Y>Z | ||
| C. | 气态氢化物的稳定性 X>Y>Z | D. | 原子最外层电子数Z>Y>X |
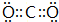 ;
;