题目内容
8.砹是原子序数最大的卤族元素,推测砹和砹的化合物不可能具有的性质是( )| A. | 砹是有色固体 | B. | 砹易溶于有机溶剂 | ||
| C. | 砹化氢很稳定 | D. | 砹化银不溶于水 |
分析 砹是原子序数最大的卤族元素,利用ⅤⅡA元素性质的相似性和递变性来解答.
解答 解:A.同主族从上到下元素的单质从气态、液态、固态变化,且颜色加深,则砹是有色固体,故A正确;
B.由碘易溶于于有机溶剂,则砹易溶于某些有机溶剂,故B正确;
C.同主族从上到下元素非金属性在减弱,则HAt很不稳定,故C错误;
D.因AgCl不溶于水,同主族元素的化合物的性质相似,则AgAt不溶于水,故D正确;
故选C.
点评 本题考查元素周期律,题目较简单,熟悉第ⅤⅡA族元素的性质变化规律即可解答,B为学生解答中的易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列物质的溶解度随温度的升高而减少的是( )
| A. | KNO3 | B. | Ca(OH)2 | C. | BaSO4 | D. | AgCl |
13.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).
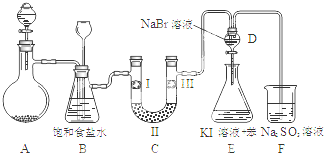
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象锥形瓶中液面下降,长颈漏斗中液面上升.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入d.
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为深棕红色,说明氯的非金属性大于溴.打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是E中溶液分为两层,上层(苯层)为紫红色.该现象不能说明溴的非金属性强于碘 (填“能”或“不能”),原因是过量的Cl2也可将I-氧化为I2.

(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象锥形瓶中液面下降,长颈漏斗中液面上升.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入d.
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
18.下列说法正确的是 ( )
| A. | 已知 ,X与Y互为同分异构体,可用FeCl3溶液鉴别 ,X与Y互为同分异构体,可用FeCl3溶液鉴别 | |
| B. |  能发生的反应类型:加成反应、取代反应、消去反应、水解反应 能发生的反应类型:加成反应、取代反应、消去反应、水解反应 | |
| C. | 3-甲基-3-乙基戊烷的一氯代物有3种 | |
| D. | 相同条件下乙酸乙酯在水中的溶解度比其在乙醇中的溶解度大 |
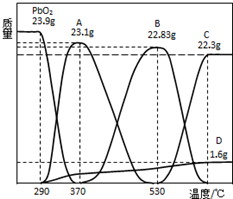 某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$2PbSO4(s)+2H2O(l)
某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$2PbSO4(s)+2H2O(l)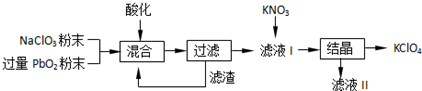
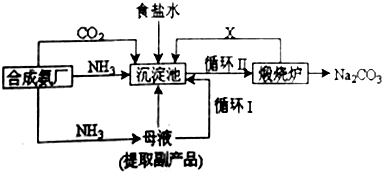
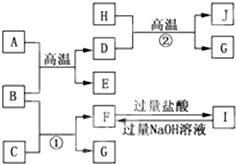 如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体.
如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体.