题目内容
下列变化中,需要加入氧化剂才能实现的是( )
| A、HCl→H2 |
| B、FeO→Fe2+ |
| C、SO2→SO3 |
| D、CO32-→CO2 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:需要加入氧化剂才能实现说明选项中的物质作还原剂,在氧化还原反应失电子化合价升高,据此分析解答.
解答:
解:需要加入氧化剂才能实现说明选选项中的物质作还原剂,在氧化还原反应失电子化合价升高,
A.HCl→H2中H元素化合价由+1价变为0价,所以HCl作氧化剂,故A错误;
B.FeO→Fe2+中Fe元素化合价都是+2价,所以FeO既不是氧化剂也不是还原剂,故B错误;
C.SO2→SO3中S元素化合价由+4价变为+6价,所以二氧化硫作还原剂,故C正确;
D.CO32-→CO2中C、O元素化合价都不变,所以碳酸根离子既不是氧化剂又不是还原剂,故D错误;
故选C.
A.HCl→H2中H元素化合价由+1价变为0价,所以HCl作氧化剂,故A错误;
B.FeO→Fe2+中Fe元素化合价都是+2价,所以FeO既不是氧化剂也不是还原剂,故B错误;
C.SO2→SO3中S元素化合价由+4价变为+6价,所以二氧化硫作还原剂,故C正确;
D.CO32-→CO2中C、O元素化合价都不变,所以碳酸根离子既不是氧化剂又不是还原剂,故D错误;
故选C.
点评:本题考查了氧化还原反应,根据元素化合价变化及基本概念来分析解答,题目难度不大.

练习册系列答案
相关题目
下列叙述不正确的是( )
| A、与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 |
| B、氨盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处 |
| C、化学键可以使离子相结合,也可以使原子相结合 |
| D、离子键、共价键、氢键都属于化学键 |
在常温下,pH=3的盐酸与pH=11的某一元碱等体积混合,所得溶液的pH( )
| A、等于7 | B、小于或等于7 |
| C、大于或等于7 | D、无法确定 |
下列有关焓(H)判据和熵(S)判据的叙述正确的是( )
| A、△H>0的反应使体系能量升高,不能自发进行 |
| B、△H<0的反应使体系能量降低,无需加热便能自发进行 |
| C、在与外界隔离的体系中,自发过程将导致熵增大 |
| D、熵增原理说明△S<0过程在任何条件下都不能自发进行 |
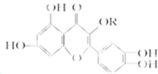 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A、可以和溴水反应 |
| B、可用有机溶剂萃取 |
| C、1mol 维生素P可以和7mol H2反应 |
| D、1mol 维生素P可以和4mol NaOH反应 |
 已知在一定条件下,2mol H2完全燃烧生成液态水时放出热量572kJ,请回答下列问题:
已知在一定条件下,2mol H2完全燃烧生成液态水时放出热量572kJ,请回答下列问题: