题目内容
氯气和氯乙烯都是非常重要的化工产品,年产量均在107t左右,氯气的实验室制备和氯乙烯的工业生产都有多种不同方法.
完成下列填空:
(1)实验室制取纯净的氯气,除了二氧化锰、浓盐酸和浓硫酸,还需要 、 (填写试剂或溶液名称)
(2)实验室用2.00mol/L盐酸和漂粉精[成分为Ca(ClO)2、CaCl2]反应生成氯气、氯化钙和水,若产生2.24L(标准状况)氯气,发生反应的盐酸为 mL.
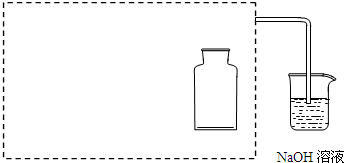
(3)实验室通常用向上排空气法收集氯气.设计一个简单实验,验证所收集的氯气中是否含有空气.
工业上用电石-乙炔生产氯乙烯的反应如下:
CaO+3C
CaC2+CO
CaC2+2H2O→HC≡CH↑+Ca(OH)2
HC≡CH+HCl
CH2═CHCl
电石-乙炔法的优点是流程简单,产品纯度高,而且不依赖于石油资源.
电石-乙炔法的缺点是: 、 .
(4)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢.
设计一种以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示(不必注明反应条件).
要求:①反应产生的氯化氢必须用于氯乙烯的制备;②不再产生其他废液.
完成下列填空:
(1)实验室制取纯净的氯气,除了二氧化锰、浓盐酸和浓硫酸,还需要
(2)实验室用2.00mol/L盐酸和漂粉精[成分为Ca(ClO)2、CaCl2]反应生成氯气、氯化钙和水,若产生2.24L(标准状况)氯气,发生反应的盐酸为
(3)实验室通常用向上排空气法收集氯气.设计一个简单实验,验证所收集的氯气中是否含有空气.
工业上用电石-乙炔生产氯乙烯的反应如下:
CaO+3C
| 2200℃~2300℃ |
CaC2+2H2O→HC≡CH↑+Ca(OH)2
HC≡CH+HCl
| HgCl2 |
| 140℃~200℃ |
电石-乙炔法的优点是流程简单,产品纯度高,而且不依赖于石油资源.
电石-乙炔法的缺点是:
(4)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢.
设计一种以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示(不必注明反应条件).
要求:①反应产生的氯化氢必须用于氯乙烯的制备;②不再产生其他废液.
考点:真题集萃,氯气的实验室制法,制备实验方案的设计
专题:实验设计题
分析:(1)实验室制备纯净的氯气,应用饱和氯化钠溶液除去HCl,用氢氧化钠溶液进行尾气吸收;
(2)反应的方程式为ClO-+Cl-+2H+=Cl2↑+H2O,n(Cl2)=
=0.1mol,结合反应的方程式计算;
(3)氯气可与氢氧化钠溶液反应,如含有空气,则与氢氧化钠反应后试管内有残留气体;用电石生产乙炔,耗能大,且污染环境;
(4)以乙烯和氯气为原料制取氯乙烯,可由乙烯和氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生消去反应生成氯乙烯,生成的氯化氢电解生成氢气和氯气,氢气和乙烯发生加成反应生成乙烷,乙烷和氯气发生取代反应生成1,2-二氯乙烷.
(2)反应的方程式为ClO-+Cl-+2H+=Cl2↑+H2O,n(Cl2)=
| 2.24L |
| 22.4L/mol |
(3)氯气可与氢氧化钠溶液反应,如含有空气,则与氢氧化钠反应后试管内有残留气体;用电石生产乙炔,耗能大,且污染环境;
(4)以乙烯和氯气为原料制取氯乙烯,可由乙烯和氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生消去反应生成氯乙烯,生成的氯化氢电解生成氢气和氯气,氢气和乙烯发生加成反应生成乙烷,乙烷和氯气发生取代反应生成1,2-二氯乙烷.
解答:
解:(1)实验室用盐酸制备氯气,氯气中混有氯化氢,得到纯净的氯气,应用饱和氯化钠溶液除去HCl,再用浓硫酸干燥,最后用氢氧化钠溶液进行尾气吸收,
故答案为:饱和食盐水;烧碱溶液;
(2)反应的方程式为ClO-+Cl-+2H+=Cl2↑+H2O,n(Cl2)=
=0.1mol,则需要n(HCl)=0.2mol,
发生反应的盐酸的体积为
=0.1L=100mL,
故答案为:100;
(3)氯气可与氢氧化钠溶液反应,如含有空气,则与氢氧化钠反应后试管内有残留气体;
工业在高温下生产电石,用电石生产乙炔,耗能大,由于乙炔与HCl的反应在氯化汞的作用下进行,污染环境,
故答案为:将集气瓶倒置于有足量烧碱溶液的水槽里,若气体不能充满集气瓶,液面上有无色气体,则有空气,若充满,则无空气;反应温度高,能耗大;使用的催化剂毒性大;
(4)以乙烯和氯气为原料制取氯乙烯,可由乙烯和氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生消去反应生成氯乙烯,生成的氯化氢电解生成氢气和氯气,氢气和乙烯发生加成反应生成乙烷,乙烷和氯气发生取代反应生成1,2-二氯乙烷,涉及反应有CH2=CH2+Cl2→CH2ClCH2Cl CH2ClCH2Cl
CH2=CHCl+HCl;
2 HCl
H2↑+Cl2↑; CH2=CH2+H2
CH3CH3;CH3CH3+Cl2→CH2ClCH2Cl,
故答案为:CH2=CH2+Cl2→CH2ClCH2Cl CH2ClCH2Cl
CH2=CHCl+HCl;2 HCl
H2↑+Cl2↑; CH2=CH2+H2
CH3CH3;CH3CH3+Cl2→CH2ClCH2Cl.
故答案为:饱和食盐水;烧碱溶液;
(2)反应的方程式为ClO-+Cl-+2H+=Cl2↑+H2O,n(Cl2)=
| 2.24L |
| 22.4L/mol |
发生反应的盐酸的体积为
| 0.2mol |
| 2mol/L |
故答案为:100;
(3)氯气可与氢氧化钠溶液反应,如含有空气,则与氢氧化钠反应后试管内有残留气体;
工业在高温下生产电石,用电石生产乙炔,耗能大,由于乙炔与HCl的反应在氯化汞的作用下进行,污染环境,
故答案为:将集气瓶倒置于有足量烧碱溶液的水槽里,若气体不能充满集气瓶,液面上有无色气体,则有空气,若充满,则无空气;反应温度高,能耗大;使用的催化剂毒性大;
(4)以乙烯和氯气为原料制取氯乙烯,可由乙烯和氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生消去反应生成氯乙烯,生成的氯化氢电解生成氢气和氯气,氢气和乙烯发生加成反应生成乙烷,乙烷和氯气发生取代反应生成1,2-二氯乙烷,涉及反应有CH2=CH2+Cl2→CH2ClCH2Cl CH2ClCH2Cl
| △ |
2 HCl
| ||
| 催化剂 |
| △ |
故答案为:CH2=CH2+Cl2→CH2ClCH2Cl CH2ClCH2Cl
| △ |
| ||
| 催化剂 |
| △ |
点评:本题为2014年上海考题,考查氯气的实验室制备以及实验方案的设计,侧重于学生的分析能力、计算能力和实验能力的考查,注意把握实验的原理以及题给信息,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
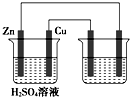 如图用铜锌原电池(电解质溶液为稀硫酸)在铁棒上电镀铜,下列叙述正确的是( )
如图用铜锌原电池(电解质溶液为稀硫酸)在铁棒上电镀铜,下列叙述正确的是( )| A、铜在原电池中作负极,在电镀池中作阳极 |
| B、原电池溶液增加的质量比电镀池阴极增加的质量大 |
| C、锌棒每减少0.65 g,导线上转移的电子约为1.204×1022个 |
| D、电路中电子的移动方向是从Zn沿导线到电镀池的铜极,再经过溶液到铁棒 |
20mL 1mol/L NaCl溶液和40mL 0.5mol/L MgCl2溶液混合之后(体积的变化忽略不计),混合液中Cl-的物质的量浓度为( )
| A、0.5 mol/L |
| B、0.6 mol/L |
| C、1 mol/L |
| D、2 mol/L |
下列结论错误的是( )
①微粒半径:K+>Al3+>S2->C1-
②氢化物的稳定性:HF>HC1>H2S>PH3>SiH4
③离子的还原性:S2->C1->Br->I-
④氧化性:C12>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
①微粒半径:K+>Al3+>S2->C1-
②氢化物的稳定性:HF>HC1>H2S>PH3>SiH4
③离子的还原性:S2->C1->Br->I-
④氧化性:C12>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A、只有① | B、①③ |
| C、②④⑤ | D、①③⑤ |
下列变化中,需要加入氧化剂才能实现的是( )
| A、HCl→H2 |
| B、FeO→Fe2+ |
| C、SO2→SO3 |
| D、CO32-→CO2 |
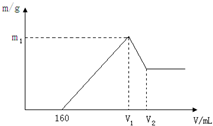 将镁铝的混合物0.1mol溶于100mL 2mol?L-1硫酸溶液中,然后再滴加1mol?L-1氢氧化钠溶液,请回答以下问题:
将镁铝的混合物0.1mol溶于100mL 2mol?L-1硫酸溶液中,然后再滴加1mol?L-1氢氧化钠溶液,请回答以下问题: