题目内容
50mL l8mol/L的硫酸与足量铜片共热,被还原的硫酸的物质的量是( )
| A、大于0.9 mol |
| B、等于0.45 mol |
| C、小于0.45mol |
| D、大于0.45 mol小于0.9 mol |
考点:浓硫酸的性质
专题:氧族元素
分析:铜与浓硫酸加热时发生反应,随着反应的进行,浓硫酸的浓度逐渐减小,当成为稀硫酸是此反应停止.
解答:
解:50ml 18mol/L的硫酸中n(H2SO4)=18mol/L×0.05L=0.9mol,假设50ml 18mol/L的硫酸中的硫酸分子全部与铜反应时,据Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O可知作氧化剂的硫酸为0.45mol,起酸作用的硫酸0.45mol,随着反应的进行,浓硫酸溶液的浓度逐渐减小,当成为稀硫酸是此反应停止,所以作氧化剂的硫酸的物质的量小于0.45mol,即被还原的硫酸的物质的量小于0.45mol,
故选:C.
| ||
故选:C.
点评:本题考查了Cu与浓硫酸的反应,注意量变会引起质变,同样的物质由于浓度不同,反应就不同,题目难度不大.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
下列关于有机物的叙述正确的是( )
| A、乙醇不能发生取代反应 |
| B、C4H10 有三种同分异构体 |
| C、氨基酸、淀粉均属于高分子化合物 |
| D、通过红外光谱分析可以区分乙醇和乙酸乙酯 |
白蚁分泌的蚁酸的化学性质与盐酸相似,能腐蚀很多建筑材料.下列材料中最不容易被白蚁蛀蚀的是( )
| A、钢 | B、铜 | C、大理石 | D、生铁 |
如图,用阿斯匹林与扑热息痛可制备一种解热镇痛抗炎药--贝诺酯.有关叙述错误的是( )

| A、扑热息痛的某种同分异构体可发生缩聚反应 |
| B、1mol阿斯匹林最多可消耗2mol NaOH |
| C、贝诺酯在碱性条件下完全水解最多可得到四种有机物 |
| D、用Na2CO3 溶液可鉴别阿斯匹林和扑热息痛 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1molFe被完全氧化生成Fe2O3,失去个3NA电子 |
| B、78gNa2O2含有阴、阳离子总数是4NA[M(Na2O2)=78g/mol] |
| C、0.1mol?L-1的MgCl2中有NA个Mg2+ |
| D、标准状况下,22.4L盐酸含有NA个HCl分子 |
已知甲、乙两种物质的溶解度(S甲、S乙)均随着温度的升高而增大.在10℃时20g水中最多能溶解5克甲;30℃时,乙物质的饱和溶液中溶质的质量分数为20%,则20℃时S甲和S乙比较,正确的是( )
| A、S甲=S乙 |
| B、S甲>S乙 |
| C、S甲<S乙 |
| D、无法确定 |
下列化学用语表达正确的是( )
A、NH4Cl的电子式: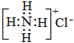 | ||
B、具有16个质子、16个中子和18个电子的微粒是
| ||
C、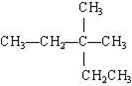 的名称为:2-甲基-2-乙基丁烷 的名称为:2-甲基-2-乙基丁烷 | ||
D、硝基苯的结构简式: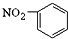 |
下列可证明甲烷分子是正四面体结构的是( )
| A、一氯甲烷没有同分异构体 |
| B、二氯甲烷没有同分异构体 |
| C、甲烷分子的四个键完全相同 |
| D、甲烷分子的四个键完全不相同 |