题目内容
1.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 1molHCl溶液中,H+数目为NA | |
| B. | 常温常压下,8gCH4含有电子数目为5NA | |
| C. | 12gNaHSO4晶体中含有0.3NA个阳离子 | |
| D. | 78g苯含有C=C双键的数目为3 NA |
分析 A、在盐酸溶液中,除了HCl能电离出氢离子,水也能电离出氢离子;
B、求出甲烷的物质的量,然后根据1mol甲烷中含10mol电子;
C、求出硫酸氢钠的物质的量,然后根据1mol硫酸氢钠晶体中含1mol钠离子和1mol硫酸氢根来分析;
D、苯不是单双键交替的结构.
解答 解:A、在盐酸溶液中,除了HCl能电离出氢离子,水也能电离出氢离子,故溶液中的氢离子个数多于NA个,故A错误;
B、8g甲烷的物质的量为0.5mol,而1mol甲烷中含10mol电子,故0.5mol甲烷中含5NA个电子,故B正确;
C、12g硫酸氢钠的物质的量为0.1mol,而1mol硫酸氢钠晶体中含1mol钠离子和1mol硫酸氢根,故0.1mol硫酸氢钠中含0.1NA个阳离子,故C错误;
D、苯不是单双键交替的结构,故苯中不含碳碳双键,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
11.下列电子排布式或轨道表示式正确的是( )
①C原子的轨道表示式: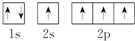
②Cr原子的电子排布式:1s22s22p63s23p63d44s2
③O原子的轨道表示式: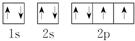
④Br原子的外围电子排布式:3d104s24p5
⑤B原子的轨道表示式: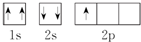
①C原子的轨道表示式:

②Cr原子的电子排布式:1s22s22p63s23p63d44s2
③O原子的轨道表示式:

④Br原子的外围电子排布式:3d104s24p5
⑤B原子的轨道表示式:

| A. | ①②③ | B. | ②③④ | C. | ①②④⑤ | D. | 只有③ |
16.若甲烷与溴蒸气以物质的量之比1:3混合,在光照下得到的有机产物:
①CH3Br
②CH2Br2
③CHBr3
④CBr4,
其中正确的是( )
①CH3Br
②CH2Br2
③CHBr3
④CBr4,
其中正确的是( )
| A. | 只有① | B. | 只有③ | C. | ①②③的混合物 | D. | ①②③④的混合物 |
6.由16个质子、18个中子、18个电子构成的微粒是( )
| A. | 分子 | B. | 原子 | C. | 阴离子 | D. | 阳离子 |
10.逻辑推理是化学学习中常用的一种思维方式,以下推理中正确的是( )
| A. | 化合物都是由不同元素组成的,故不同元素组成的物质一定是化合物 | |
| B. | 在金属活动性顺序表中排在氢元素前的金属能与酸反应放出氢气,金属镁排在氢的前面,所以金属镁一定与硝酸反应放出氢气 | |
| C. | 有新物质生成的变化属于化学变化,所以化学变化一定有新物质生成 | |
| D. | 单质都是由一种元素组成的,所以由一种元素组成的物质一定是单质 |
11. 向100mL 0.1mol/L AlCl3 溶液中,加入c mol/L NaOH 溶液100mL后,再滴加1mol/L 盐酸,滴加盐酸的体积与生成沉淀的质量关系如图所示,则加入的NaOH溶液的浓度为( )
向100mL 0.1mol/L AlCl3 溶液中,加入c mol/L NaOH 溶液100mL后,再滴加1mol/L 盐酸,滴加盐酸的体积与生成沉淀的质量关系如图所示,则加入的NaOH溶液的浓度为( )
 向100mL 0.1mol/L AlCl3 溶液中,加入c mol/L NaOH 溶液100mL后,再滴加1mol/L 盐酸,滴加盐酸的体积与生成沉淀的质量关系如图所示,则加入的NaOH溶液的浓度为( )
向100mL 0.1mol/L AlCl3 溶液中,加入c mol/L NaOH 溶液100mL后,再滴加1mol/L 盐酸,滴加盐酸的体积与生成沉淀的质量关系如图所示,则加入的NaOH溶液的浓度为( )| A. | 0.25mol/L | B. | 2mol/L | C. | 1mol/L | D. | 0.5 mol/L |