��Ŀ����
8������ʵ���Ӧ�������۾���ȷ�����߾��������ϵ���ǣ�������| ѡ��[�� | ʵ�� | ���� | ���� |
| A | �����£������ȱ������AlƬ�ֱ�͵����ϡHNO3��ŨHNO3��Ӧ | ǰ�߲�����ɫ���壬���߲�������ɫ���壬�Һ��߷�Ӧ���Ӿ��� | ����������ͬʱ����Ӧ��Ũ��Խ��Ӧ����Խ�� |
| B | FeCl3��Һ���ڿ�ʴͭ��ӡˢ��·�� | ��Һ���� | �����ԣ�Cu2+��Fe2+ |
| C | ��FeCl2��Һ�м�������Na2O2��ĩ | ���ֺ��ɫ��������ɫ���� | FeCl2��Һ���ֱ��� |
| D | �����������۵�FeI2��Һ�еμ�2����ˮ | ��Һ���� | ��ԭ�ԣ�I-��Fe2+ |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��AlƬ��ϡHNO3����������ԭ��Ӧ����NO����ŨHNO3��AlƬ�����ۻ���
B��FeCl3��Һ���ڿ�ʴͭ��ӡˢ��·�壬ͭ��FeCl3��Һ����������ԭ��Ӧ�����Ȼ�ͭ���Ȼ������������������������Դ������������жϣ�
C���������ƾ���ǿ�����ԣ��������������ӣ�
D����ˮ�����������ӣ��ⵥ�������۱��������ݻ�ԭ���Ļ�ԭ�Դ��ڻ�ԭ�����жϣ�
��� �⣺A��AlƬ��ϡHNO3����������ԭ��Ӧ������ɫ����NO����ŨHNO3��AlƬ�����ۻ�������ɫ���壬����������A����
B��FeCl3��Һ���ڿ�ʴͭ��ӡˢ��·�壬ͭ��FeCl3��Һ����������ԭ��Ӧ�����Ȼ�ͭ���Ȼ���������������Fe3+��Cu2+�����۴���B����
C���������ƾ���ǿ�����ԣ��������������ӣ�����˵��FeCl2��Һ���ֱ��ʣ���C����
D����ˮ�����������ӣ��ⵥ�������۱��������������֪��ԭ��I-��Fe2+����D��ȷ��
��ѡD��
���� ���⿼�黯ѧʵ�鷽�������ۣ�Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ������Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ʵ��������Է�������Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
16������˵����ȷ���ǣ�������
| A�� | ú�ĸ����ǻ�ѧ�仯����ú��������Һ���������仯 | |
| B�� | ʯ���ѽ���Ϊ�˻�ø������ͣ�������Ѹ��������������Ҫ | |
| C�� | ���ܡ����ܡ����ܶ�����������Ⱦ����ɫ����Դ������ȫʹ�� | |
| D�� | �����ǽ�ʯ��ʯ�����ʯӢ�ڲ�����¯�и��������Ƶõ� |
20��λ��Ԫ�����ڱ��еڶ�����IVA���Ԫ���ǣ�������
| A�� | ̼ | B�� | �� | C�� | �� | D�� | �� |
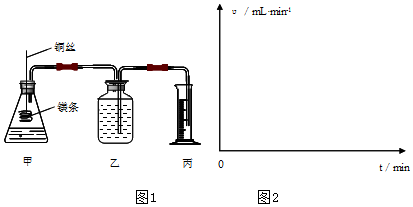
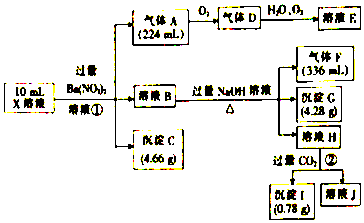
3����ҵ̼���ƣ�����ԼΪ98%���г�����Ca2+��Mg2+��Fe3+��Cl����SO42�������ʣ�Ϊ���ᴿ��ҵ̼���ƣ�������Լ���̼���ƣ���ȡ����������ͼ1��ʾ��

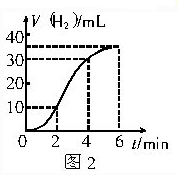
��֪����̼���Ƶı�����Һ�ڲ�ͬ�¶���������������ͼ2��ʾ��
���й����ʵ��ܶȻ�����
��1������NaOH��Һ��ҪΪ�˳�ȥMg2+�������ӷ��ţ���������Ӧ�����ӷ���ʽΪMgCO3+2OH-=Mg��OH ��2��+CO32-��������������Ҫ�ɷ���Mg��OH��2��Fe��OH��3��CaCO3���ѧʽ���� ����Mg2+��Fe3+����Һ�еμ�NaOH��Һ�������ֳ�����������Һ��pH=8ʱ��c��Mg2+����c��Fe3+��=2.125��1021��
��2���ȵ�Na2CO3��Һ�н�ǿ��ȥ������������ԭ���ǣ������ӷ���ʽ����Ҫ�����ּ��Խ��ͣ�Na2CO3����Һ�д���ˮ��ƽ��CO32-+H2O?HCO3-+OH-����Һ�ʼ��ԣ����¶�����ʱˮ��ƽ�������ƶ���ʹ��Һ������ǿ����ȥ����������ǿ��
��3�������ȹ��ˡ�ʱ���¶�Ӧ�����ڸ���36�森
��4����֪��Na2CO3•10H2O��s���TNa2CO3��s��+10H2O��g����H=+532.36kJ•mol-1
Na2CO3•10H2O��s���TNa2CO3•H2O��s��+9H2O��g����H=+473.63kJ•mol-1
д��Na2CO3•H2O��ˮ��Ӧ���Ȼ�ѧ����ʽNa2CO3•H2O��S���TNa2CO3��s��+H2O��g����H=+58.73kJ/mol��
��5�����˴ӡ���ɫ��ѧ���Ƕ����뽫��ĸҺ��������ͼ��������ʾ����ѭ��ʹ�ã��������ʵ���������Ƿ���в����У�������������ĸҺ��ѭ��ʹ�ã�����Һc��Cl-����c��SO42-������������ò���Na2CO3�л������ʣ�

��֪����̼���Ƶı�����Һ�ڲ�ͬ�¶���������������ͼ2��ʾ��
���й����ʵ��ܶȻ�����
| ���� | CaCO3 | MgCO3 | Ca��OH��2 | Mg��OH��2 | Fe��OH��3 |
| Ksp | 4.96��10-9 | 6.82��10-6 | 4.68��10-6 | 5.61��10-12 | 2.64��10-39 |
��2���ȵ�Na2CO3��Һ�н�ǿ��ȥ������������ԭ���ǣ������ӷ���ʽ����Ҫ�����ּ��Խ��ͣ�Na2CO3����Һ�д���ˮ��ƽ��CO32-+H2O?HCO3-+OH-����Һ�ʼ��ԣ����¶�����ʱˮ��ƽ�������ƶ���ʹ��Һ������ǿ����ȥ����������ǿ��
��3�������ȹ��ˡ�ʱ���¶�Ӧ�����ڸ���36�森
��4����֪��Na2CO3•10H2O��s���TNa2CO3��s��+10H2O��g����H=+532.36kJ•mol-1
Na2CO3•10H2O��s���TNa2CO3•H2O��s��+9H2O��g����H=+473.63kJ•mol-1
д��Na2CO3•H2O��ˮ��Ӧ���Ȼ�ѧ����ʽNa2CO3•H2O��S���TNa2CO3��s��+H2O��g����H=+58.73kJ/mol��
��5�����˴ӡ���ɫ��ѧ���Ƕ����뽫��ĸҺ��������ͼ��������ʾ����ѭ��ʹ�ã��������ʵ���������Ƿ���в����У�������������ĸҺ��ѭ��ʹ�ã�����Һc��Cl-����c��SO42-������������ò���Na2CO3�л������ʣ�

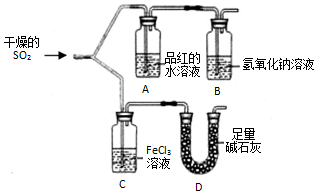 ��ͼװ�ý���SO2��������ʵ�飮
��ͼװ�ý���SO2��������ʵ�飮