题目内容
己知向NaNO2溶液中加入酸性KMn04溶液发生如下反应:2KMn04+5NaNO2+3H2S04=2MnSO4+5NaNO3+K2SO4+3H2O 有关该反应的下列说法中正确的是( )
| A、KMn04作氧化剂 |
| B、该反应不属于离子反应 |
| C、氮元素被还原 |
| D、当反应中转移10 mol电子时,生成lmol MnS04 |
考点:氧化还原反应
专题:
分析:反应2KMnO4+5KNO2+3H2SO4=5KNO3+2MnSO4+K2SO4+3H2O中,Mn元素化合价降低,被还原,KMnO4为氧化剂,N元素化合价升高,被氧化,KNO2为还原剂,以此解答该题.
解答:
解:反应2KMnO4+5KNO2+3H2SO4=5KNO3+2MnSO4+K2SO4+3H2O中,Mn元素化合价降低,被还原,KMnO4为氧化剂,N元素化合价升高,被氧化,KNO2为还原剂;
A.由分析可知KMn04作氧化剂,故A正确;
B.反应在溶液中进行,有离子参加,属于离子反应,故B错误;
C.反应中N元素化合价升高,被氧化,故C错误;
D.反应中Mn元素化合价从+7价降低到+2价,每当生成lmol MnS04,转移5mol电子,故D错误;
故选A.
A.由分析可知KMn04作氧化剂,故A正确;
B.反应在溶液中进行,有离子参加,属于离子反应,故B错误;
C.反应中N元素化合价升高,被氧化,故C错误;
D.反应中Mn元素化合价从+7价降低到+2价,每当生成lmol MnS04,转移5mol电子,故D错误;
故选A.
点评:本题考查氧化还原反应,侧重于学生的分析能力和基本概念的理解和运用的考查,注意从元素化合价的角度认识相关概念及相关物质的性质的判断,难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
已知NaHSO3溶液显酸性,溶液中存在以下平衡:HSO3-+H2O?H2SO3+OH-①HSO3-?H++SO32-②,向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
| A、加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 | ||||||||
B、加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+
| ||||||||
C、加入少量NaOH溶液,
| ||||||||
| D、加入氨水至中性,则2c(Na+)=c(SO32-)>c(H+)=c(OH-) |
下列物质中只含有离子键的是( )
| A、CaCl2 |
| B、C2H4 |
| C、N2 |
| D、Na202 |
氢原子的3d和4s能级的能量高低是( )
| A、3d>4s |
| B、3d<4s |
| C、3d=4s |
| D、无3d、4s轨道,无所谓能量高低 |
科学家预测原子序数为114的元素具有相当的稳定性,它的位置在第7周期ⅣA族,称为类铅,下列关于它的性质预测中,错误的是( )
| A、它的最外层电子数为4 |
| B、它的金属性比硅强 |
| C、它具有7个电子层 |
| D、它的最高价氧化物的水化物是强酸 |
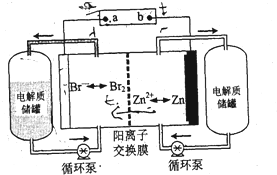 锌溴液流电池是一种新型电化学储能装置(如图所示)电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示)电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )| A、充电时电极b连接电源的正极 |
| B、放电时正极的电极反应式为Zn-2e-=Zn2+ |
| C、阳离子交换膜可阻止Br2与Zn直接发生反应 |
| D、充电时左侧电解质储罐中的离子总浓度增大 |

