题目内容
电解质溶液中相关粒子浓度的大小关系.
(1)同一溶液中不同离子浓度的大小比较
①NH4Cl溶液中的c(NH4+)、c(H+)、c(OH-)、c(Cl-)大小关系
②NaHCO3溶液中的c(Na+)、c(H+)、c(HCO3-)、c(OH-)大小关系
(2)不同溶液中同一离子浓度的大小比较
①物质的量浓度相同的下列溶液中,c(NH4+)由大到小的顺序是
A.(NH4)2SO4 B.(NH4)2CO3 C.(NH4)2Fe(SO4)2
②c(NH4+)相等的①NH4Cl ②NH4HCO3 ③NH4HSO4 三种溶液中,溶质浓度由大到小的顺序是 .
(1)同一溶液中不同离子浓度的大小比较
①NH4Cl溶液中的c(NH4+)、c(H+)、c(OH-)、c(Cl-)大小关系
②NaHCO3溶液中的c(Na+)、c(H+)、c(HCO3-)、c(OH-)大小关系
(2)不同溶液中同一离子浓度的大小比较
①物质的量浓度相同的下列溶液中,c(NH4+)由大到小的顺序是
A.(NH4)2SO4 B.(NH4)2CO3 C.(NH4)2Fe(SO4)2
②c(NH4+)相等的①NH4Cl ②NH4HCO3 ③NH4HSO4 三种溶液中,溶质浓度由大到小的顺序是
考点:离子浓度大小的比较,盐类水解的应用
专题:盐类的水解专题
分析:(1)①氯化铵为强酸弱碱盐,铵根离子水解导致溶液呈酸性,溶液中存在电荷守恒,根据电荷守恒判断;
②碳酸氢钠中碳酸氢根离子水解程度大于电离程度,所以溶液呈碱性,碳酸氢根离子水解但程度较小,钠离子不水解,根据物料守恒判断;
(2)①碳酸根离子促进铵根离子水解、亚铁离子抑制铵根离子水解,铵根离子水解程度越大,溶液中c(NH4+)越小;
②碳酸氢根离子促进铵根离子水解、氢离子抑制铵根离子水解,铵根离子水解程度越大,相同c(NH4+)的铵盐浓度越大.
②碳酸氢钠中碳酸氢根离子水解程度大于电离程度,所以溶液呈碱性,碳酸氢根离子水解但程度较小,钠离子不水解,根据物料守恒判断;
(2)①碳酸根离子促进铵根离子水解、亚铁离子抑制铵根离子水解,铵根离子水解程度越大,溶液中c(NH4+)越小;
②碳酸氢根离子促进铵根离子水解、氢离子抑制铵根离子水解,铵根离子水解程度越大,相同c(NH4+)的铵盐浓度越大.
解答:
解:(1)①氯化铵为强酸弱碱盐,铵根离子水解导致溶液呈酸性,则c(H+)>c(OH-),溶液中存在电荷守恒,根据电荷守恒得c(NH4+)<c(Cl-),铵根离子水解程度较小,所以溶液中c(H+) 较小,则离子浓度大小顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-),故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
②碳酸氢钠中碳酸氢根离子水解程度大于电离程度,所以溶液呈碱性,则c(H+)<c(OH-),碳酸氢根离子水解但程度较小,钠离子不水解,根据物料守恒得c(Na+)>c(HCO3-),所以离子浓度大小顺序是c(Na+)>c(HCO3-)>c(OH-)>c(H+),故答案为:c(Na+)>c(HCO3-)>c(OH-)>c(H+);
(2)①碳酸根离子促进铵根离子水解、亚铁离子抑制铵根离子水解,铵根离子水解程度越大,溶液中c(NH4+)越小,所以c(NH4+)由大到小的顺序是C>A>B,故答案为:C>A>B;
②碳酸氢根离子促进铵根离子水解、氢离子抑制铵根离子水解,铵根离子水解程度越大,相同c(NH4+)的铵盐浓度越大,所以c(NH4+)相同的这三种溶液溶质浓度由大到小的顺序是②>①>③,故答案为:②>①>③.
②碳酸氢钠中碳酸氢根离子水解程度大于电离程度,所以溶液呈碱性,则c(H+)<c(OH-),碳酸氢根离子水解但程度较小,钠离子不水解,根据物料守恒得c(Na+)>c(HCO3-),所以离子浓度大小顺序是c(Na+)>c(HCO3-)>c(OH-)>c(H+),故答案为:c(Na+)>c(HCO3-)>c(OH-)>c(H+);
(2)①碳酸根离子促进铵根离子水解、亚铁离子抑制铵根离子水解,铵根离子水解程度越大,溶液中c(NH4+)越小,所以c(NH4+)由大到小的顺序是C>A>B,故答案为:C>A>B;
②碳酸氢根离子促进铵根离子水解、氢离子抑制铵根离子水解,铵根离子水解程度越大,相同c(NH4+)的铵盐浓度越大,所以c(NH4+)相同的这三种溶液溶质浓度由大到小的顺序是②>①>③,故答案为:②>①>③.
点评:本题考查离子浓度大小比较,明确溶质的性质确定溶液酸碱性,再结合守恒思想分析解答,注意(2)离子之间的相互影响,题目难度中等.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
(双项)青苹果汁遇到碘酒时显蓝色,熟苹果汁能与Cu(OH)2悬浊液反应生成砖红色沉淀,这说明( )
| A、青苹果中含有淀粉 |
| B、熟苹果中只含单糖 |
| C、苹果转熟时单糖聚合成淀粉 |
| D、苹果转熟时淀粉水解为葡萄糖 |
50mL BaCl2溶液所含有的Cl-,与20mL 0.5mol?L-1的硝酸银溶液恰好完全反应,则原溶液BaCl2的物质的量的浓度是( )
| A、1 mol?L-1 |
| B、0.8 mol?L-1 |
| C、0.2 mol?L-1 |
| D、0.1 mol?L-1 |
下列有关强电解质叙述正确的是( )
| A、电解质溶液在电流作用下电离成阴离子和阳离子 |
| B、强电解质在熔化状态下一定能够导电 |
| C、具有强极性键的共价化合物可能是强电解质 |
| D、强电解质的水溶液一定具有很强的导电能力 |
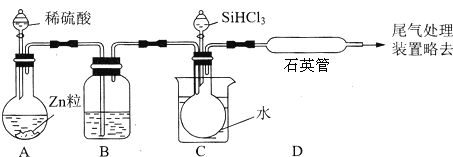


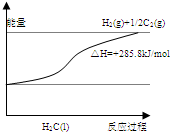 A、B、C、D、E是原子序数依次增大的前四周期元素,其信息如表:
A、B、C、D、E是原子序数依次增大的前四周期元素,其信息如表: