题目内容
19.下列各组离子一定能大量共存的是( )| A. | 在无色溶液中:NH4+、Fe2+、SO42-、CO32- | |
| B. | 在含大量Fe3+溶液中:NH4+、Na+、Cl-、SCN- | |
| C. | 在强碱溶液中:Na+、K+、Cl-、SO32- | |
| D. | 使石蕊变红色的溶液中:K+、Fe2+、Cl-、CH3COO- |
分析 A.Fe2+为浅绿色;
B.离子之间结合生成络离子;
C.强碱溶液中该组离子之间不反应;
D.使石蕊变红色的溶液,可显酸性.
解答 解:A.Fe2+为浅绿色,与无色不符,且Fe2+、CO32-结合生成沉淀,不能共存,故A不选;
B.Fe3+、SCN-结合生成络离子,不能共存,故B错误;
C.强碱溶液中该组离子之间不反应,可大量共存,故C正确;
D.使石蕊变红色的溶液,可显酸性,酸性溶液中不能大量存在CH3COO-,故D错误;
故选C.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、络合反应的判断,题目难度不大.

练习册系列答案
相关题目
16.X、Y、Z、W为四种短周期主族元素.其中X、Z同主族,Y、Z同周期,W与X、Y既不同主族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6.下列说法正确的是( )
| A. | Y、Z两元素的简单离子半径Y>Z | |
| B. | X与W可以形成W2X、W2X2两种化合物 | |
| C. | X、Y、Z对应气态氢化物的热稳定性和还原性强弱顺序一致 | |
| D. | Y、Z元素最高价氧化物对应的水化物酸性较强的为H2ZO4 |
10.下列叙述正确的是( )
| A. | 钠在氧气中燃烧,火焰呈黄色,产生白色固体 | |
| B. | 屠呦呦利用乙醇萃取青蒿汁中的青蒿素,获得了2015年度诺贝尔医学奖,为人类防治疟疾作出了重大贡献 | |
| C. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| D. | 镁燃烧发出耀眼的白光,常用于制造信号弹和焰火 |
7.下列说法正确的是( )
| A. | 花生油是纯净物 | B. | 油脂是甘油和高级脂肪酸的混合物 | ||
| C. | 动物脂肪和矿物油都属于油脂 | D. | 同种单甘油酯可组成纯净物 |
14.下列基团表示方法正确的是( )
| A. | 乙基 CH2CH3 | B. | 硝基-NO3 | C. | 苯基 | D. | 羟基  |
4.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
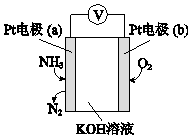

| A. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| B. | 电极a的反应式为2NH3-6e-+6OH-═N2+6H2O | |
| C. | O2在电极b上发生还原反应 | |
| D. | 溶液中OH-向电极a移动 |
9.人们对原子结构的认识有一个不断深入的过程,其中提出“葡萄干面包”原子模型的科学家是( )
| A. | 道尔顿 | B. | 汤姆生 | C. | 卢瑟福 | D. | 玻尔 |