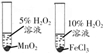
题目内容
5.工业上按下列路线合成结构简式为的物质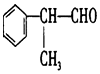 ,该物质是一种香料.
,该物质是一种香料.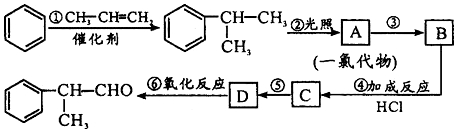
请根据上述路线,回答下列问题:
(1)A的结构简式可能为:
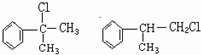 ;
;(2)反应①、③、⑤的反应类型分别为加成、消去、取代或水解;
(3)写出下列反应④、⑥的化学方程式为(要求:有机物写结构简式,并注明反应条件):
④
 ;⑥2
;⑥2 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2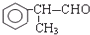 +2H2O.
+2H2O.(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化D的方法,其原因是
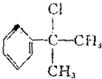 的水解产物
的水解产物 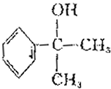 中的-OH不在链端,不能氧化成-CHO.
中的-OH不在链端,不能氧化成-CHO.(5)这种香料具有多种同分异构体,其中某些物质有下列特征:
①该物质的水溶液遇FeCl3溶液呈紫色;
②分子中有苯环,且苯环上的一溴代物有两种.
写出符号上述条件的物质可能的结构简式(只写两种):
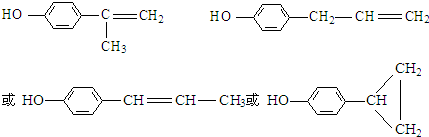 .
.
分析 反应①是苯与丙烯发生加成反应生成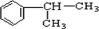 ,在光照条件下
,在光照条件下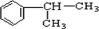 可与氯气发生取代反应生成A为
可与氯气发生取代反应生成A为 ,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为
,B与HCl发生信息中的加成反应,氯原子连接在含氢较多的碳原子上,则A应发生消去反应生成B为 ,则C为
,则C为 ,结合根据产物可知D为
,结合根据产物可知D为 ,以此解答该题.
,以此解答该题.
解答 解:(1)通过以上分析知,A为 ,故答案为:
,故答案为: ;
;
(2)反应①为加成反应,反应③为A发生消去反应生成 ,⑤为
,⑤为 发生取代反应或水解反应生成
发生取代反应或水解反应生成 ,
,
故答案为:加成;消去;取代或水解;
(3)反应④的化学方程式为: ,
,
反应⑥的化学方程式为2 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2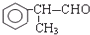 +2H2O,
+2H2O,
故答案为: ;2
;2 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2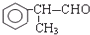 +2H2O;
+2H2O;
(4)A为 ,D为
,D为 ,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法的原因是:A中
,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法的原因是:A中  的水解产物
的水解产物  中的-OH不在链端,不能氧化成-CHO,
中的-OH不在链端,不能氧化成-CHO,
故答案为: 的水解产物
的水解产物  中的-OH不在链端,不能氧化成-CHO;
中的-OH不在链端,不能氧化成-CHO;
(5)①该物质的水溶液遇FeCl3溶液呈紫色,说明含有酚羟基,
②分子中有苯环,且苯环上的一溴代物有两种,则苯环上有2个取代基,且位于对位位置,可能为则符合条件的 的同分异构体有:
的同分异构体有: ,
,
故答案为: .
.
点评 本题考查了有机物的推断,为高考常见题型,明确有机物的官能团、性质及其反应条件是解本题关键,反应物相同条件不同导致产物不同,方程式和同分异构体的书写是常考查点,难点是同分异构体的书写,书写时不能重复、不能漏写,总结书写方法和方式,题目难度中等.

练习册系列答案
相关题目
15.下列粒子的结构示意图中,表示钠原子的是( )
| A. | 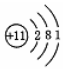 | B. | 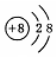 | C. | 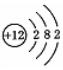 | D. | 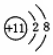 |
13.关于氯化铁溶液,下列有关说法正确的是( )
| A. | 适当升高温度能促进FeCl3水解 | |
| B. | 加水稀释能促进其水解,并提高Fe(OH)3的浓度 | |
| C. | 加少量浓盐酸能促进FeCl3水解 | |
| D. | 保存氯化铁溶液时应加入少量铁粉 |
20.下列物质的工业生产原理不涉及氧化还原反应的是( )
| A. | 氨气 | B. | 纯碱 | C. | 硫酸 | D. | 烧碱 |
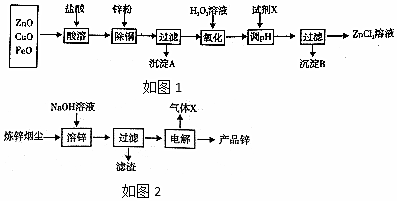
10.以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氧化锌和金属锌.
Ⅰ.制取氧化锌主要工艺如图1:
表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算).
(1)为了加快反应,“酸溶”需要适当加热,但温度不宜太高,原因是减少盐酸挥发.
(2)加入H2O2溶液发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)流程图中,为了降低溶液的酸度,调节pH范围为3.2≤PH<5.2;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为3Zn2(OH)2CO3+4Fe3++3H2O=4Fe(OH)3↓+6Zn2++3CO2↑.
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为4.0×10-5.从ZnCl2溶液中提取无水ZnCl2的方法是在氯化氢气体,蒸干氯化锌溶液并加热至失去结晶水.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O═Na2[Zn(OH)4](aq),然后电解浸取液.
(5)如图2,炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
(6)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
Ⅰ.制取氧化锌主要工艺如图1:

表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
(2)加入H2O2溶液发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)流程图中,为了降低溶液的酸度,调节pH范围为3.2≤PH<5.2;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为3Zn2(OH)2CO3+4Fe3++3H2O=4Fe(OH)3↓+6Zn2++3CO2↑.
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为4.0×10-5.从ZnCl2溶液中提取无水ZnCl2的方法是在氯化氢气体,蒸干氯化锌溶液并加热至失去结晶水.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O═Na2[Zn(OH)4](aq),然后电解浸取液.
(5)如图2,炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
(6)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
17.“同位素示踪法,可帮助人们认识化学反应的机理.下列反应中同位素示踪表示正确的是( )
| A. | 2Na2O2+2H218O═4NaOH+18O2↑ | |
| B. | K37ClO3+6HCl═K37Cl+3Cl2↑+3H2O | |
| C. | NH4Cl+2H2O?NH3•2H2O+HCl | |
| D. | CH3COOH+CH3CH218OH$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O |
14.化学与科学、技术、社会、环境密切相关.下列说法不正确的是( )
| A. | 为加快漂白精的漂白速率,使用时可滴加几滴醋酸 | |
| B. | 在食品袋中放人盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| C. | 用含橙色酸性重铬酸钾的仪器检验酒驾,利用了乙醇的挥发性和还原性 | |
| D. | 光太阳能电池先将光能转化为化学能,然后再将化学能转化为电能 |
15.有一种军用烟幕弹中装有ZnO、Al粉和C2Cl6,其发烟过程中的化学反应如下:
①3ZnO+2Al→Al2O3+3Zn ②3Zn+C2Cl6→3ZnCl2+2C
下列有关叙述不正确的是( )
①3ZnO+2Al→Al2O3+3Zn ②3Zn+C2Cl6→3ZnCl2+2C
下列有关叙述不正确的是( )
| A. | 反应①是铝热反应 | B. | 反应②是置换反应 | C. | C2Cl6属于卤代烃 | D. | 氧化性:Al<Zn<C |