题目内容
2.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.说法正确的是( )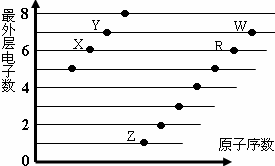
| A. | 元素非金属性:X>R>W | |
| B. | X与R形成的分子内含两种作用力 | |
| C. | X、Z形成的化合物中可能含有共价键 | |
| D. | 元素对应的离子半径:W>R>X |
分析 都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,结合对应单质、化合物的性质以及元素周期律知识解答该题.
解答 解:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,
A.同周期元素从左到右非金属性逐渐增强,应为Cl>S,故A错误;
B.X与R形成的分子可为SO2或SO3,分子内只存在极性键,故B错误;
C.X、Z形成的化合物如为Na2O2,可含有共价键,故C正确;
D.核外电子排布相同的离子核电荷数越大离子半径越小,半径Cl-<S2-,故D错误.
故选C.
点评 本题考查原子结构与元素周期律知识,为高考常见题型和高频考点,侧重于学生的分析能力的考查,根据最外层电子数及原子序数的关系确定元素是解题的关键,注意整体把握元素周期表的结构,难度中等.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
10.尿素燃料电池既能去除城市废水中的尿素,又能发电.尿素燃料电池结构如图所示,甲电极上发生如下反应:CO(NH2)2+H2O-6e→CO2+N2+6H+,则( )
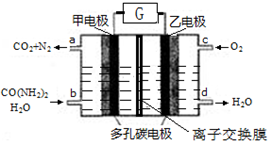

| A. | 甲电极是阴极 | B. | 电解质溶液可以是KOH溶液 | ||
| C. | H+从甲电极附近向乙电极附近迁移 | D. | 每2molO2理论上可净化1molCO(NH2)2 |
17.三氟化溴溶于水可发生反应3BrF3+5H2O→HBrO3+Br2+9HF+O2↑,下列说法正确的是( )
| A. | 氧化产物是O2 | |
| B. | BrF3既是氧化剂又是还原剂 | |
| C. | 当有5mol水参加反应,生成22.4L氧气 | |
| D. | 当反应中转移3NA个电子时,有NA个水分子被氧化 |
7.已知某溶液中含有碳酸钠、硫酸钠、氢氧化钠、氯化钠四种溶质,欲将该溶液中四种溶质的阴离子逐一检验出来,所加试剂先后顺序合理的是( )
| A. | HNO3、Ba(NO3)2、NH4NO3、AgNO3 | B. | HNO3、NH4NO3、Ba(NO3)2、AgNO3 | ||
| C. | NH4NO3、HNO3、Ba(NO3)2、AgNO3 | D. | NH4NO3、HNO3、AgNO3、Ba(NO3)2 |
12.EDTA是一种重要的络合剂.4mol 一氯乙酸和1mol乙二胺(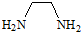 )在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( )
)在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( )
 )在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( )
)在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( )| A. | C10H16N2O8 | B. | C10H20N2O8 | C. | C8H16N2O8 | D. | C16H20N2O8Cl |
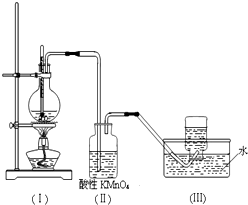 如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后观察到烧瓶中溶液变黑,装置(Ⅱ)中经硫酸酸化的高锰酸钾溶液褪色.
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后观察到烧瓶中溶液变黑,装置(Ⅱ)中经硫酸酸化的高锰酸钾溶液褪色.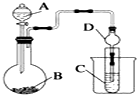 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验. 科研人员对某岛上山泉水进行分析化验,结果显示山泉水属于硬水.
科研人员对某岛上山泉水进行分析化验,结果显示山泉水属于硬水.