题目内容
12.EDTA是一种重要的络合剂.4mol 一氯乙酸和1mol乙二胺(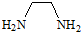 )在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( )
)在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( )| A. | C10H16N2O8 | B. | C10H20N2O8 | C. | C8H16N2O8 | D. | C16H20N2O8Cl |
分析 一氯乙酸的结构简式为CH2ClCOOH,乙二胺的分子式为C2H8N2,结合反应的方程式利用质量守恒可确定EDTA的分子式.
解答 解:一氯乙酸的结构简式为CH2ClCOOH,分子式为C2H3O2Cl,乙二胺的分子式为C2H8N2,
4mol 一氯乙酸和1mol乙二胺( )在一定条件下发生反应生成1mol EDTA和4mol HCl,
)在一定条件下发生反应生成1mol EDTA和4mol HCl,
则有4C2H3O2Cl+C2H8N2→EDTA+4HCl,
由质量守恒可知EDTA的分子式为C10H16N2O8,
故选A.
点评 本题考查有机物分子式的计算,侧重于学生的分析能力的考查,注意解答本题可根据反应的关系式利用质量守恒计算,难度不大.

练习册系列答案
相关题目
2.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.说法正确的是( )
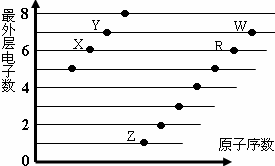

| A. | 元素非金属性:X>R>W | |
| B. | X与R形成的分子内含两种作用力 | |
| C. | X、Z形成的化合物中可能含有共价键 | |
| D. | 元素对应的离子半径:W>R>X |
20.3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2△H>0.下列说法正确的是( )
| A. | 元素H的单质存在H2、D2、T2三种同素异形体 | |
| B. | 在该反应条件下,H2的还原性强于Fe的还原性 | |
| C. | 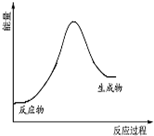 该反应的能量变化关系可以用如图表示 | |
| D. | 1molFe与水蒸气完全反应转移的电子数为3×6.02×1023 |
17.天然气脱硫的方法有多种,一种是干法脱硫,其涉及的反应:H2(g)+CO(g)+SO2(g)?H2O(g)+CO2(g)+S(s)+Q(Q>0).要提高脱硫率可采取的措施是( )
| A. | 加催化剂 | B. | 分离出硫 | C. | 减压 | D. | 加生石灰 |
4.如表实验不能达到预期实验目的是( )
| 序号 | 实验操作 | 实验目的 |
| A | 在浓硫酸和稀硫酸中分别加入Cu片,加热 | 比较稀、浓硫酸氧化性强弱 |
| B | F2、Cl2分别与H2反应 | 比较氟、氯的非金属性强弱 |
| C | 把CO2通入到水玻璃中 | 比较碳、硅的非金属性强弱 |
| D | 向MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
1.下列各组中的性质比较,不正确的是( )
| A. | 水溶性:SO2>Cl2>CO2 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 稳定性:NH3>H2O>HF | D. | 沸点:F2<Cl2<Br2<I2 |
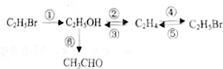
 ②CH3CH2OH
②CH3CH2OH CH2=CH2↑+H2O
CH2=CH2↑+H2O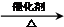 CH3CH2Br 乙醛的银镜反应
CH3CH2Br 乙醛的银镜反应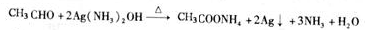
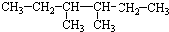 .
.