题目内容
20.在下列各组物质中,分子数一定相同的是( )| A. | 0.2mol H2和4.48L HCl气体 | B. | 标准状况下1mol O2和22.4L H2O | ||
| C. | 2g 氦气和标准状况下11.2L CO2 | D. | 4L CO和4L CO2 |
分析 根据N=nNA可知,物质的分子数一定相同,则二者的物质的量相等,根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$进行计算即可,注意标准状况下气体摩尔体积的使用条件.
解答 解:根据N=nNA可知,物质的分子数一定相同,说明二者的物质的量相等,
A.没有告诉在标准状况下,不能使用标准状况下的气体摩尔体积计算HCl的物质的量,则二者的物质的量不一定相等,故A错误;
B.标准状况下水的状态不是气态,不能使用标准状况下的气体摩尔体积计算水的物质的量,则二者的物质的量不相等,故B错误;
C.2g氦气的物质的量为:$\frac{2g}{4g/mol}$=0.5mol,标准状况下11.2L二氧化碳的物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,二者的物质的量相等,则含有的分子数相等,故C正确;
D.没有告诉在相同条件下,气体摩尔体积不一定相等,则二者的物质的量不一定相等,故D错误;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确标准状况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积之间的关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.对于平衡体系:aA(g)+bB(g)?cC(g)+dD(g)△H<0,下列判断中正确的是( )
| A. | 若a+b<c+d,增大压强,则平衡向左移动 | |
| B. | 若从正反应开始,起始时A、B的物质的量之比为a:b,则平衡时A、B的转化率之比为a:b | |
| C. | 若a+b=c+d,在平衡体系中共有气体m mol,再向其中充入n mol B,则达到平衡时气体总物质的量小于(m+n)mol | |
| D. | 若a+b=c+d,则对于体积不变的容器,升高温度,平衡向左移动,容器中气体压强不变 |
11.(1)在微生物作用的条件下,NH4+ 经过两步反应被氧化成NO3-.两步反应的能量变化示意图如图:
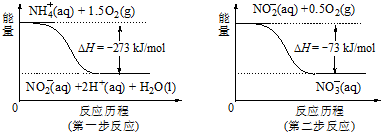
①第一步反应是放热反应(选题“放热”或“吸热”),判断依据是反应物的总能量大于生成物的总能量
②1mol NH4+(aq)全部氧化成NO3- (aq)的热化学方程式是NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol
(2)用酸式滴定管准确移取25.00mL某未知浓度的盐酸于一洁净的锥形瓶中,然后用0.20mol•L-1的氢氧化钠溶液(指示剂为酚酞)滴定,滴定结果如下:
①滴定管在使用之前需要先查漏,再洗涤和润洗
②判断滴定终点的现象是无色变粉红色,且半分钟内不变色
③根据以上数据可以计算出盐酸的物质的量浓度为0.15 mol•L-1(小数点后保留两位有效数字).
④以下操作可能造成测定结果偏高的是ACE(填写序号).
A.滴定前,碱式滴定管尖嘴有气泡,滴定后消失
B.滴定前读数正确,达到滴定终点后,俯视读数
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管
(3)由pH=3的HA(弱酸)与pH=11的NaOH溶液等体积混合,所得溶液中离子浓度大小的顺序为c(A-)>c(Na+)>c(H+)>c(OH-).

①第一步反应是放热反应(选题“放热”或“吸热”),判断依据是反应物的总能量大于生成物的总能量
②1mol NH4+(aq)全部氧化成NO3- (aq)的热化学方程式是NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol
(2)用酸式滴定管准确移取25.00mL某未知浓度的盐酸于一洁净的锥形瓶中,然后用0.20mol•L-1的氢氧化钠溶液(指示剂为酚酞)滴定,滴定结果如下:
| 实验编号 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.40mL |
| 第二次 | 3.00mL | 21.10mL |
| 第三次 | 0.20mL | 20.40mL |
| 第四次 | 0.00mL | 18.20mL |
②判断滴定终点的现象是无色变粉红色,且半分钟内不变色
③根据以上数据可以计算出盐酸的物质的量浓度为0.15 mol•L-1(小数点后保留两位有效数字).
④以下操作可能造成测定结果偏高的是ACE(填写序号).
A.滴定前,碱式滴定管尖嘴有气泡,滴定后消失
B.滴定前读数正确,达到滴定终点后,俯视读数
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管
(3)由pH=3的HA(弱酸)与pH=11的NaOH溶液等体积混合,所得溶液中离子浓度大小的顺序为c(A-)>c(Na+)>c(H+)>c(OH-).
5.在密闭容器中充入A(g)和B(g),它们的初始浓度均为2mol•L-1,在一定条件下发生反应:A(g)+B(g)?2C(g).该温度下,此反应的平衡常数为4,则A的转化率为( )
| A. | 30% | B. | 40% | C. | 50% | D. | 60% |
12.摩尔是表示( )
| A. | 物质的量的单位 | B. | 物质的质量的单位 | ||
| C. | 物质的量的浓度 | D. | 摩尔质量的单位 |
9.对于一定不能自发进行的反应来说,反应后体系的( )
| A. | 混乱度增大,而能量降低 | B. | 混乱度降低,而能量增大 | ||
| C. | 混乱度降低,而能量降低 | D. | 混乱度增大,而能量增大 |
10.下列无色透明的溶液中能大量共存的一组离子是( )
| A. | Na+、Cu2+、Cl-、SO42- | B. | H+、Na+、Fe2+、NO3- | ||
| C. | K+、Mg2+、Cl-、SO42- | D. | K+、Fe3+、SCN-、SO42- |