题目内容
10.下列无色透明的溶液中能大量共存的一组离子是( )| A. | Na+、Cu2+、Cl-、SO42- | B. | H+、Na+、Fe2+、NO3- | ||
| C. | K+、Mg2+、Cl-、SO42- | D. | K+、Fe3+、SCN-、SO42- |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.Cu2+为蓝色,与无色不符,故A不选;
B.H+、Fe2+、NO3-发生氧化还原反应,不能共存,故B不选;
C.该组离子之间不反应,可大量共存,且离子均为无色,故C选;
D.Fe3+、SCN-结合生成络离子不能共存,且Fe3+为黄色,与无色不符,故D不选;
故选C.
点评 本题考查离子共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
20.在下列各组物质中,分子数一定相同的是( )
| A. | 0.2mol H2和4.48L HCl气体 | B. | 标准状况下1mol O2和22.4L H2O | ||
| C. | 2g 氦气和标准状况下11.2L CO2 | D. | 4L CO和4L CO2 |
1.化学概念在逻辑上存在如图关系,对下列概念的说法正确的是( )
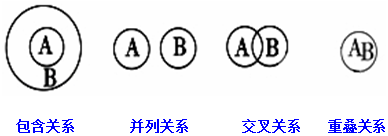

| A. | 化合物与氧化物属于交叉关系 | B. | 单质与非电解质属于包含关系 | ||
| C. | 溶液与分散系属于并列关系 | D. | 化合物与电解质属于包含关系 |
18.对外加电流的金属保护中,被保护的金属( )
| A. | 与电源的正极相连 | B. | 表面上发生氧化反应 | ||
| C. | 与电源的负极相连 | D. | 与另一种活泼性较差的金属相连 |
5.如图所示,下列实验操作与方法不正确的是( )
| A. | 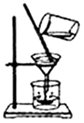 过滤 | B. | 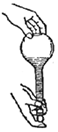 检查容量瓶是否漏水 | ||
| C. | 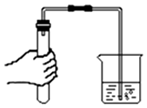 气密性检查 | D. | 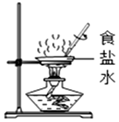 蒸发 |
15.下列解释事实的化学方程式或离子方程式不正确的是( )
| A. | 工业上可角电解法制备Mg:MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+C12↑ | |
| B. | 用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+Fe2++14H+═2Cr3++Fe3++7H2O | |
| C. | 用CaSO4治理盐碱地:CaSO4(s)+Na2CO3(aq)?CaCO3(s)+Na2SO4(aq) | |
| D. | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2═2HClO+CaCO3↓ |
2.下列溶液中Cl-物质的量浓度与25mL1mol/L AlCl3溶液的Cl-物质的量浓度相等的是( )
| A. | 100mL2.5mol/L NaCl溶液 | B. | 200mL2mol/L MgCl2溶液 | ||
| C. | 300mL3mol/L KCl溶液 | D. | 150mL2mol/L AlCl3溶液 |
19.下列有关有机化合物的说法正确的是( )
| A. | 乙烷室温下能与浓盐酸发生取代反应 | |
| B. | 由乙烯生成乙醇属于加成反应 | |
| C. | C4H9Cl有3种同分异构体 | |
| D. | 油脂和蛋白质都属于高分子化合物 |
 有机化工原料溴乙烷的沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是CH3CH2OH+HBr→CH3CH2Br+H2O.
有机化工原料溴乙烷的沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是CH3CH2OH+HBr→CH3CH2Br+H2O.