题目内容
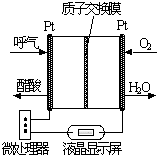
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH
2K2CO3+6H2O

(1)请回答图中:甲电池是 装置,
(2)请回答下列电极的名称:A(石墨)电极的名称是 .
(3)写出通入CH3OH的电极的电极反应式是 .
(4)乙池中反应的化学方程式为 .
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下).
| 放电 |
| 充电 |

(1)请回答图中:甲电池是
(2)请回答下列电极的名称:A(石墨)电极的名称是
(3)写出通入CH3OH的电极的电极反应式是
(4)乙池中反应的化学方程式为
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)甲装置为燃料电池;
(2)A与原电池的正极相连;
(3)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水;B电极与原电池负极相连,为阴极,银离子在B上得电子;
(4)乙为电解池,电解质溶液为AgNO3;
(5)根据电极方程式计算.
(2)A与原电池的正极相连;
(3)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水;B电极与原电池负极相连,为阴极,银离子在B上得电子;
(4)乙为电解池,电解质溶液为AgNO3;
(5)根据电极方程式计算.
解答:
解:(1)甲装置为甲醇燃料电池,属于原电池,
故答案为:原电池;
(2)A与原电池的正极相连,则A为阳极;
故答案为:阳极;
(3)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,其电极的电极反应式是CH3OH-6e-+8OH-═6H2O+CO32-;B电极与原电池负极相连,为阴极,银离子在B上得电子,其电极方程式为:Ag++e-=Ag;
故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;Ag++e-=Ag;
(4)乙为电解池,电解质溶液为AgNO3,则乙池中反应的化学方程式为4AgNO3+2H2O
4Ag+O2↑+4HNO3,
故答案为:4AgNO3+2H2O
4Ag+O2↑+4HNO3;
(5)乙池中A(Ag)极上银离子得电子生成Ag,其电极反应为Ag++e-=Ag,已知A(Ag)极的质量增加5.40g时,n(Ag)=0.05mol,
则转移电子为0.05mol,甲中正极反应为:O2+4e-+H2O=4OH-,则转移0.05mol电子时消耗的氧气为0.0125mol,则氧气的体积为0.0125mol×22.4L/mol=0.28L=280ml
故答案为:280.
故答案为:原电池;
(2)A与原电池的正极相连,则A为阳极;
故答案为:阳极;
(3)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,其电极的电极反应式是CH3OH-6e-+8OH-═6H2O+CO32-;B电极与原电池负极相连,为阴极,银离子在B上得电子,其电极方程式为:Ag++e-=Ag;
故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;Ag++e-=Ag;
(4)乙为电解池,电解质溶液为AgNO3,则乙池中反应的化学方程式为4AgNO3+2H2O
| ||
故答案为:4AgNO3+2H2O
| ||
(5)乙池中A(Ag)极上银离子得电子生成Ag,其电极反应为Ag++e-=Ag,已知A(Ag)极的质量增加5.40g时,n(Ag)=0.05mol,
则转移电子为0.05mol,甲中正极反应为:O2+4e-+H2O=4OH-,则转移0.05mol电子时消耗的氧气为0.0125mol,则氧气的体积为0.0125mol×22.4L/mol=0.28L=280ml
故答案为:280.
点评:本题考查了原电池和电解池原理,明确离子放电顺序是解本题关键,难点是电极反应式的书写,题目难度中等.

练习册系列答案
相关题目
某NaCl和CaCl2的混合溶液中,c(Ca2+)=0.2mol?L-1,c(Cl-)=0.7mol?L-1,那么c(Na+)为( )
| A、0.1 mol?L-1 |
| B、0.2 mol?L-1 |
| C、0.3 mol?L-1 |
| D、0.4 mol?L-1 |
溶液和胶体具备的共同性质是( )
| A、分散质微粒都能透过半透膜 |
| B、用石墨电极做导电性实验时,分散质微粒都定向且朝一个方向移动 |
| C、都有丁达尔现象 |
| D、都比较稳定 |
 研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.