题目内容
下列反应不属于氧化还原反应的是( )
| A、Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O |
| B、Cu+2FeCl3═CuCl2+2FeCl2 |
| C、HCl+NaHCO3=NaCl+H2O+CO2↑ |
| D、3Cl2+6NaOH=5NaCl+NaClO3+3H2O |
考点:氧化还原反应
专题:氧化还原反应专题
分析:不属于氧化还原反应,说明该反应中没有电子转移,即没有元素化合价变化,据此分析解答.
解答:
解:A.该反应中Cu元素化合价由0价变为+2价、N元素化合价由+5价变为+4价,所以属于氧化还原反应,故A错误;
B.该反应中Cu元素化合价由0价变为+2价、Fe元素化合价由+3价变为+2价,所以有电子转移,属于氧化还原反应,故B错误;
C.该反应中各元素化合价都不变,不属于氧化还原反应,属于复分解反应,故C正确;
D.该反应中Cl元素化合价由0价变为-1价、+5价,所以有电子转移,属于氧化还原反应,故D错误;
故选C.
B.该反应中Cu元素化合价由0价变为+2价、Fe元素化合价由+3价变为+2价,所以有电子转移,属于氧化还原反应,故B错误;
C.该反应中各元素化合价都不变,不属于氧化还原反应,属于复分解反应,故C正确;
D.该反应中Cl元素化合价由0价变为-1价、+5价,所以有电子转移,属于氧化还原反应,故D错误;
故选C.
点评:本题考查了氧化还原反应判断,根据反应中元素化合价是否变化来分析解答,知道常见元素化合价,题目难度不大.

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
 一些简单原子的原子结构可用如图①、②、③形象地表示:根据该图的示意,则下列有关图①、②、③所表示的原子叙述正确的是( )
一些简单原子的原子结构可用如图①、②、③形象地表示:根据该图的示意,则下列有关图①、②、③所表示的原子叙述正确的是( )| A、①②③互为同位素 |
| B、①②③互为同素异形体 |
| C、①②③为同种原子 |
| D、①②③具有相同的质量数 |
催化剂的研究是化学反应原理中的一个重要领域,下列有关叙述正确的是( )
| A、加催化剂可以增大或减小化学反应的焓变 |
| B、某反应的△H=+100 kJ?mol-1,则正反应活化能比逆反应活化能小100 kJ?mol-1 |
| C、任何化学反应都需要活化能的推动 |
| D、对于在给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的比例 |
有下列三个反应:①Cl2+FeI2═FeCl2+I2 ②2Fe2++Br2═2Fe3++2Br- ③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O.下列说法正确的是( )
| A、①②③中的氧化产物分别是I2、Fe3+、CoCl2 |
| B、根据以上方程式可以得到还原性Co2+>Cl->Br- |
| C、可以推理得到Br2+FeI2═FeBr2+I2 |
| D、在反应③中当1mol Co2O3参加反应时,6mol HCl被氧化 |
下列有关试剂的保存方法正确的是.( )
①NaOH固体保存在配有橡皮塞的细口瓶中;
②Na2CO3溶液通常保存在配有橡皮塞的细口瓶中;
③液溴通常用水封保存;
④白磷保存在煤油中;
⑤浓硝酸通常保存在棕色细口瓶中.
①NaOH固体保存在配有橡皮塞的细口瓶中;
②Na2CO3溶液通常保存在配有橡皮塞的细口瓶中;
③液溴通常用水封保存;
④白磷保存在煤油中;
⑤浓硝酸通常保存在棕色细口瓶中.
| A、①③⑤ | B、②③⑤ |
| C、②④⑤ | D、①③④ |
标准状况下,下列物质体积最大的是( )
| A、2gH2 |
| B、20gSO2 |
| C、23gNa |
| D、160gBr2 |
下列操作正确且能达到预期目的是( )
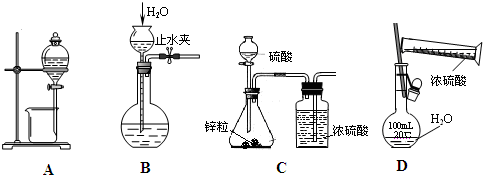

| A、分离酒精和水 |
| B、检查气体发生装置的气密性 |
| C、用Zn粒和稀硫酸制备干燥的H2 |
| D、用浓硫酸配制100mL 1.0mol/L的稀硫酸 |
0.1mol/L的NH4Cl溶液中,下列离子浓度大小比较正确的是( )
| A、C(NH4+)>C(Cl-)>C(H+)>C(OH-) |
| B、C(Cl-)>C(NH4+)>C(OH-)>C(H+) |
| C、C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
| D、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |