题目内容
 2014年初,雾霾天气多次肆虐我国中东部地区.加强汽车尾气排放监测和降低有毒气体的排放对于减少雾霾具有重要的意义.
2014年初,雾霾天气多次肆虐我国中东部地区.加强汽车尾气排放监测和降低有毒气体的排放对于减少雾霾具有重要的意义.(1)在汽车上安装高效催化转化器,可有效降低NOx和CO的排放.某科研小组为了测定在某种催化剂作用下[2NO(g)+2CO(g)
| 催化剂 |
| 浓度 时间/s |
0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c(NO)(×10-4mol/L) | 8.50 | 4.50 | a | 1.50 | 1.00 | 0.80 | 0.80 |
| c(CO)(×10-3mol/L) | 3.60 | 3.20 | 3.00 | b | 2.85 | 2.83 | 2.83 |
①前2s内的平均反应速率v(CO2)=
②根据该反应中反应物的浓度变化与时间的关系,判断表格中a=
③已知:N2(g)+O2(g)═2NO(g)△H=+179.5kJ/mol
2NO(g)+O2(g)═2NO2(g)△H=-112.3kJ/mol
NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234.3kJ/mol
则反应2NO(g)+2CO(g)
| 催化剂 |
(2)T℃时,向体积为2L的恒容密闭容器中开始充入0.2mol CO、0.2mol NO、2mol CO2和x mol N2,若要使反应在开始时正向进行,则x应满足的条件是
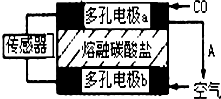
(3)利用原电池工作原理可以测定汽车尾气中CO的浓度,其装置如图所示.该电池中电解质为熔融碳酸盐,CO32-在固体介质中可以自由移动,气体A为
考点:化学平衡建立的过程,热化学方程式,化学电源新型电池
专题:基本概念与基本理论
分析:(1)①化学反应速率=
计算v(CO)的反应速率,结合反应速率之比等于化学方程式计量数之比计算v(CO2);
②依据化学平衡三段式列式计算;
③依据热化学方程式和盖斯定律计算所需让化学方程式,反应自发进行的依据是△H-T△S<0分析判断;
(2)依据浓度商和平衡常数比较分析,若要使反应在开始时正向进行,Q<K分析判断;
(3)由题意知多空电极a为负极,CO在负极发生氧化反应,多空电极b为正极,氧气在正极发生还原反应;
| △c |
| △t |
②依据化学平衡三段式列式计算;
③依据热化学方程式和盖斯定律计算所需让化学方程式,反应自发进行的依据是△H-T△S<0分析判断;
(2)依据浓度商和平衡常数比较分析,若要使反应在开始时正向进行,Q<K分析判断;
(3)由题意知多空电极a为负极,CO在负极发生氧化反应,多空电极b为正极,氧气在正极发生还原反应;
解答:
解:(1)①反应速率之比等于化学方程式计量数之比,v(CO2)=v(CO)=
=3×10-4mol/(L?s);
故答案为:3×10-4mol/(L?s);
②依据图表数据交换平衡三段式列式计算
2NO(g)+2CO(g)
2CO2(g)+N2(g)
起始量(mol/L) 8.50×10-4 3.60×10-3 0 0
变化量(mol/L) 6.0×10-46.0×10-46.0×10-4 3.0×10-4
2s量(mol/L) 2.5×10-4 3.0×10-3 6.0×10-4 3.0×10-4
2NO(g)+2CO(g)
2CO2(g)+N2(g)
起始量(mol/L) 8.50×10-4 3.60×10-3 0 0
变化量(mol/L) 7.0×10-4 7.0×10-4 7.0×10-4 3.50×10-4
3s量(mol/L) 1.5×10-4 2.9×10-3 7.0×10-4 3.50×10-4
a=2.5,b=2.9;
故答案为:2.5; 2.9;
③a、N2(g)+O2(g)═2NO(g)△H=+179.5kJ/mol
b、2NO(g)+O2(g)═2NO2(g)△H=-112.3kJ/mol
c、NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234.3kJ/mol
依据盖斯定律c×2+b-a得到,反应的热化学方程式为:2NO(g)+2CO(g)
2CO2(g)+N2(g)△H=-760.4 kJ/mol;
反应自发进行的依据是△H-T△S<0,△H<0,△S<0,满足△H-T△S<0需要在低温下;
故答案为:-760.4 kJ/mol,低温;
(2)若要使反应在开始时正向进行,Q=
<K=5×103L?mol-1
计算得到取值为:0≤x<1;
故答案为:0≤x<1;
(3)在此原电池中,CO充入负极区,CO失电子在熔融态碳酸盐中生成二氧化碳,氧气充入正极区,得电子与二氧化碳生成碳酸根,
故答案为:CO2,O2+2CO2+4e-=2CO32-;
| 3.60×10-3mol/L-3.00×10-3mol/L |
| 2s |
故答案为:3×10-4mol/(L?s);
②依据图表数据交换平衡三段式列式计算
2NO(g)+2CO(g)
| 催化剂 |
起始量(mol/L) 8.50×10-4 3.60×10-3 0 0
变化量(mol/L) 6.0×10-46.0×10-46.0×10-4 3.0×10-4
2s量(mol/L) 2.5×10-4 3.0×10-3 6.0×10-4 3.0×10-4
2NO(g)+2CO(g)
| 催化剂 |
起始量(mol/L) 8.50×10-4 3.60×10-3 0 0
变化量(mol/L) 7.0×10-4 7.0×10-4 7.0×10-4 3.50×10-4
3s量(mol/L) 1.5×10-4 2.9×10-3 7.0×10-4 3.50×10-4
a=2.5,b=2.9;
故答案为:2.5; 2.9;
③a、N2(g)+O2(g)═2NO(g)△H=+179.5kJ/mol
b、2NO(g)+O2(g)═2NO2(g)△H=-112.3kJ/mol
c、NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234.3kJ/mol
依据盖斯定律c×2+b-a得到,反应的热化学方程式为:2NO(g)+2CO(g)
| 催化剂 |
反应自发进行的依据是△H-T△S<0,△H<0,△S<0,满足△H-T△S<0需要在低温下;
故答案为:-760.4 kJ/mol,低温;
(2)若要使反应在开始时正向进行,Q=
| ||
| 0.12×0.12 |
计算得到取值为:0≤x<1;
故答案为:0≤x<1;
(3)在此原电池中,CO充入负极区,CO失电子在熔融态碳酸盐中生成二氧化碳,氧气充入正极区,得电子与二氧化碳生成碳酸根,
故答案为:CO2,O2+2CO2+4e-=2CO32-;
点评:本题考查了化学反应速率概念,平衡计算应用,热化学方程式书写方法和盖斯定律计算应用,原电池原理分析,电极书写,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
一种基于酸性燃料电池原理设计的酒精检测仪,电池反应的化学方程式为:CH3CH2OH+O2═CH3COOH+H2O.下列有关说法正确的是( )
| A、检测时,电解质溶液中的H+向负极移动 |
| B、若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C、负极上的反应为:CH3CH2OH-4e-+H2O═CH3COOH+4H+ |
| D、正极上发生的反应为:O2+4e-+2H2O═4OH- |
某有机物的结构简式为: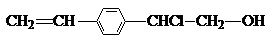
①可以燃烧②能使酸性高锰酸钾溶液褪色③能与NaOH溶液反应④能发生消去反应⑤能发生加聚反应( )
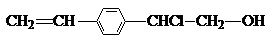
①可以燃烧②能使酸性高锰酸钾溶液褪色③能与NaOH溶液反应④能发生消去反应⑤能发生加聚反应( )
| A、只有①③ | B、只有②④⑤ |
| C、除③外 | D、全部 |
美国哥伦比亚大学的科学家根据对沉积物中稀土元素钕(Nd)的分析发现,北大西洋和太平洋海水中的
Nd和
Nd比例差异很明显,由此得出周围大陆的岩石中
Nd和
Nd含量不同的结论.下列有关说法正确的是( )
143 60 |
144 60 |
143 60 |
144 60 |
A、
| ||||
B、因各地岩石中
| ||||
C、
| ||||
| D、Nd是镧系元素,镧系元素都互为同位素 |
 我国的铜矿储量居世界第三位,主要集中在江西、云南、甘肃、湖北、安徽、西藏等.铜及其化合物在现代社会中有着极其广泛的应用.
我国的铜矿储量居世界第三位,主要集中在江西、云南、甘肃、湖北、安徽、西藏等.铜及其化合物在现代社会中有着极其广泛的应用.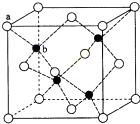 CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.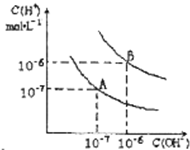 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: