题目内容
15.在短周期主族元素中,甲元素与乙、丙、丁三元素相邻,甲、乙的原子序数之和等于丙的原子序数,这四种元素原子的最外层电子数之和为20.下列判断中正确的是( )| A. | 原子半径:丙>乙>甲>丁 | |
| B. | 气态氢化物的熔点:丙>甲 | |
| C. | 乙元素在自然界中形成的化合物种类最多 | |
| D. | 乙和甲、丙、丁都一定能形成两种或两种以上的共价化合物 |
分析 甲元素与乙、丙、丁三元素相邻,甲、乙的原子序数之和等于丙的原子序数,则甲、丙同主族且丙在甲的下一周期,甲、乙、丁同周期相邻,设甲的原子最外层电子数为x,乙、丁与甲在同一周期且左右相邻,乙、丁两原子最外层电子数之和为2x,则4x=20,即x=5,所以甲是N,丙是P,乙是O,丁是C,根据元素所在周期表中的位置结合元素周期律的递变规律解答.
解答 解:甲元素与乙、丙、丁三元素相邻,甲、乙的原子序数之和等于丙的原子序数,则甲、丙同主族且丙在甲的下一周期,甲、乙、丁同周期相邻,设其原子最外层电子数为x,乙、丁与甲在同一周期且左右相邻,乙、丁两原子最外层电子数之和为2x,则4x=20,即x=5,所以甲是N,丙是P,乙是O,丁是C,
A.根据同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大,则有原子半径大小:P>C>N>O,即:丙>丁>甲>乙,故A错误;
B.甲为N、丙为P,氢化物分别为NH3、PH3,由于氨气分子中存在氢键,其沸点大于磷化氢,即沸点:甲>丙,故B错误;
C.乙为O元素,在自然界中形成的化合物种类最多的为C(丁),故C错误;
D.乙为O元素,氧元素分别能够与N、P、C形成两种或两种以上的共价化合物,故D正确;
故选D.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,正确推断元素为解答结构,注意熟练掌握原子结构与元素周期律的关系,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
6.常温时,下列叙述正确的是( )
| A. | 稀释pH=3的醋酸,溶液中所有离子的浓度均降低 | |
| B. | 相同条件下,pH=5的①NH4C1溶液、②CH3C00H溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③ | |
| C. | 体积相同、浓度均为0.1mol/L的盐酸和醋酸,分别稀释m倍、n倍,溶液的pH都变成5,则m<n | |
| D. | pH=5的硫酸溶液稀释到原来的500倍,稀释后溶液中的c(SO42-)与c(H+)之比约为1:10 |
3.二氧化硅又称硅石,是制备硅及其化合物的重要原料,下列说法正确的是( )
| A. | SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物 | |
| B. | 玛瑙和红宝石的主要成分都是SiO2,是制备半导体的材料 | |
| C. | 高温下SiO2能与Na2CO3反应放出CO2,说明硅酸酸性强于碳酸 | |
| D. | Na2SiO3溶液中逐滴加入盐酸可制备硅酸胶体 |
7.下列递变规律不正确的是( )
| A. | Na、Mg、Al的还原性依次减弱 | B. | I、Br、Cl的非金属性性依次增强 | ||
| C. | C、N、O 的原子半径依次增大 | D. | P、S、Cl的最高正化合价依次升高 |
4.某电解质溶液中有有Na+、Mg2+、Cl-、SO42-,且Na+、Mg2+、Cl-的浓度分别为0.2mol/L、0.4mol/L、0.4mol/L,则SO42-的物质的量浓度为( )
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.3mol/L | D. | 0.4mol/L |
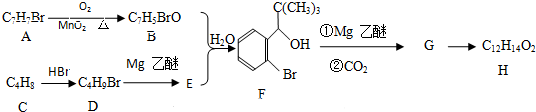
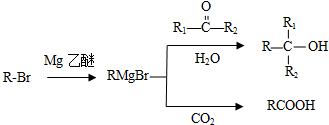
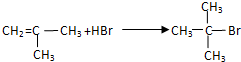 ;G→H
;G→H .
.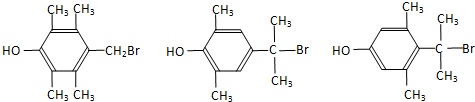 .
.
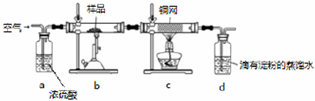
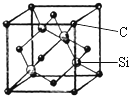 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答: