题目内容
12.下列有关化学用语表示正确的是( )| A. | NH3的电子式: | |
| B. | CS2分子的球棍模型: | |
| C. | 二氧化硅的分子式:SiO2 | |
| D. | Mg5(Si4O10)2(OH)2•4H2O的氧化物形式:5MgO•8SiO2•5H2O |
分析 A、氨气分子属于共价化合物,其分子中含有3个N-H键,N原子最外层达到8电子稳定结构;
B、S原子的半径大于C原子,且CS2的空间构型和CO2相同,为直线型;
C、二氧化硅为原子晶体,无分子式;
D、硅酸盐改写为氧化物的一般方法为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO•nSiO2•mH2O).
解答 解:A、NH3属于共价化合物,分子中存在3对共用电子对,氮原子最外层为8个电子,氨气的电子式为 ,故A错误;
,故A错误;
B、S原子的半径大于C原子,且CS2的空间构型和CO2相同,为直线型,故球棍模型为 ,故B错误;
,故B错误;
C、二氧化硅为原子晶体,无分子式,故SiO2是化学式而不是分子式,故C错误;
D、镁的氧化物为MgO,硅的氧化物为SiO2,氢的氧化物为H2O,则根据活泼金属氧化物•较活泼金属氧化物•SiO2•H2O得顺序可知,Mg3(Si4O10)(OH)2•4H2O表示为:3MgO•4SiO2•5H2O,故D正确.
故选D.
点评 本题考查了共价化合物电子式的书写、物质的球棍模型和硅酸盐改写为氧化物的方法等,综合性较强,但难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.汽车尾气排放的一氧化碳、氮氧化物等气体已成为大气污染的主要来源.德国大众汽车尾气检测造假事件引起全世界震惊.同时能源又是制约国家发展进程的因素之一.甲醇、二甲醚等被称为21世纪的绿色能源,工业上可利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
请根据如图1示意图回答(1)、(2)有关问题:
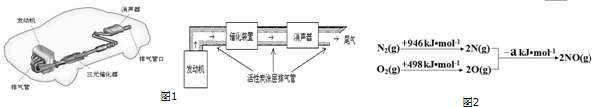
(1)汽车发动机工作时会引发N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1,其能量变化示意图如图2:
则NO中氮氧键的键能为632 kJ•mol-1.
(2)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是AD.
A.增加排气管长度 B.增大尾气排放口 C.升高排气管温度 D.添加合适的催化剂
(3)工业上一般采用下列两种反应合成甲醇:
反应a:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.5kJ•mol-1
反应b:CO (g)+2H2(g)?CH3OH(g)△H=-91.8kJ•mol-1
①对于反应a,某温度下,将4.0mol CO2(g)和12.0mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,测得甲醇蒸气的体积分数为30%,则该温度下反应的平衡常数为1.33;
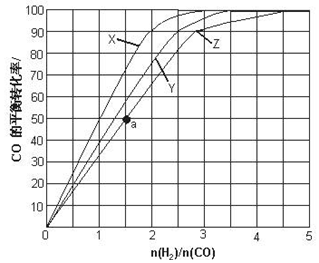
②对于反应b,在763K、3.04×104kPa时,用CO和H2做原料合成CH3OH,当原料中CO和H2的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响.设H2和CO起始物质的量之比为m,平衡时CO的转化率为α,平衡混合物中甲醇的体积分数为y,则m、α、y三者的关系式为y=$\frac{α}{1+m+2a}$
(i)请根据上述关系式将如表空白填满:
(ii)根据表中提供的数据,可得出反应物的比例对CO转化率以及平衡混合物中甲醇的体积分数影响的结论.选择最佳反应物配比是m=2,α=0.45;理由是由表中数据可知,m越大,α越大; 开始时m增大,y也随着增大,当m>2时,m增大,y减小,当m=2时,y最大 .
(4)CO可以合成二甲醚,二甲醚可以作为燃料电池的原料,化学反应原理为:
CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H<0
①在恒容密闭容器里按体积比为1:4充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是D;
A.逆反应速率先增大后减小
B.通入一定量的He,体系压强增大
C.正反应速率先减小后增大
D.化学平衡常数K值增大
②已知参与电极反应的电极材料单位质量放出电能的大小称为该电池的比能量.关于二甲醚碱性燃料电池与乙醇碱性燃料电池,下列说法正确的是AC(填字母)
A.两种燃料互为同分异构体,分子式和摩尔质量相同,但比能量不相同
B.两种燃料所含共价键数目相同,断键时所需能量相同,比能量相同
C.两种燃料所含共价键类型不同,断键时所需能量不同,比能量不同
③已知甲醇的热值是23kJ•g-1,请写出表示甲醇燃烧热的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-736kJ/mol.
请根据如图1示意图回答(1)、(2)有关问题:

(1)汽车发动机工作时会引发N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1,其能量变化示意图如图2:
则NO中氮氧键的键能为632 kJ•mol-1.
(2)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是AD.
A.增加排气管长度 B.增大尾气排放口 C.升高排气管温度 D.添加合适的催化剂
(3)工业上一般采用下列两种反应合成甲醇:
反应a:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.5kJ•mol-1
反应b:CO (g)+2H2(g)?CH3OH(g)△H=-91.8kJ•mol-1
①对于反应a,某温度下,将4.0mol CO2(g)和12.0mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,测得甲醇蒸气的体积分数为30%,则该温度下反应的平衡常数为1.33;
②对于反应b,在763K、3.04×104kPa时,用CO和H2做原料合成CH3OH,当原料中CO和H2的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响.设H2和CO起始物质的量之比为m,平衡时CO的转化率为α,平衡混合物中甲醇的体积分数为y,则m、α、y三者的关系式为y=$\frac{α}{1+m+2a}$
(i)请根据上述关系式将如表空白填满:
| m | α | y |
| 1 | 0.25 | 16.67% |
| 2 | 0.45 | |
| 3 | 0.56 | 19.35% |
(4)CO可以合成二甲醚,二甲醚可以作为燃料电池的原料,化学反应原理为:
CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H<0
①在恒容密闭容器里按体积比为1:4充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是D;
A.逆反应速率先增大后减小
B.通入一定量的He,体系压强增大
C.正反应速率先减小后增大
D.化学平衡常数K值增大
②已知参与电极反应的电极材料单位质量放出电能的大小称为该电池的比能量.关于二甲醚碱性燃料电池与乙醇碱性燃料电池,下列说法正确的是AC(填字母)
A.两种燃料互为同分异构体,分子式和摩尔质量相同,但比能量不相同
B.两种燃料所含共价键数目相同,断键时所需能量相同,比能量相同
C.两种燃料所含共价键类型不同,断键时所需能量不同,比能量不同
③已知甲醇的热值是23kJ•g-1,请写出表示甲醇燃烧热的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-736kJ/mol.
3.下列有关实验操作的叙述错误的是( )
| A. | 过滤操作中,玻璃棒应适时搅拌漏斗器 | |
| B. | 蒸发时,不能把蒸发皿放置于石棉网上加热 | |
| C. | 萃取分液时,将塞上凹槽或小孔对准漏斗上小孔,然后打开活塞才能放出下层液体 | |
| D. | 配制容量瓶,定容时改用胶头滴管滴加蒸馏水 |
20.下列仪器不宜直接用于加热的是( )
| A. | 试管 | B. | 蒸发皿 | C. | 坩埚 | D. | 烧杯 |
7.已知:常温下浓度为0.1mol/L的下列溶液的pH如表:下列有关说法不正确的是( )
| 溶质 | NaCl | Na2CO3 | NaClO | NaHCO3 |
| pH | 7 | 11.6 | 9.7 | 8.3 |
| A. | 在相同温度下,同浓度的三种酸溶液的导电能力:HCl>H2CO3>HClO | |
| B. | 等体积等物质的量浓度的NaCl溶液与NaClO溶液中Cl-和ClO-离子个数:Cl->ClO- | |
| C. | 向Na2CO3溶液中逐滴滴入少量稀盐酸,反应为:Na2CO3+2HCl=2NaCl+CO2↑+H2O | |
| D. | 若将CO2通入0.1mol/L Na2CO3溶液至溶液中性,则溶液中:2c(CO32-)+c(HCO3-)=0.2mol/L |
2. 乙醇、乙酸都是有机化工重要的基础原料.
乙醇、乙酸都是有机化工重要的基础原料.
(1)空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(2)浓硫酸催化下,乙酸和乙醇生成乙酸乙酯
CH3COOH+CH3CH2OH$?_{110-120℃}^{H_{2}SO_{4}}$CH3COOH2CH3+H2O
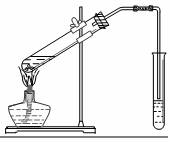
某化学兴趣小组的同学用如图装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是大试管中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙酸.
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止倒吸.
③相关物质的部分性质:
根据上表数据有同学提出可用水替代小试管中的Na2CO3溶液,你认为可行吗?说明理由:不能,乙酸乙酯在乙醇、乙酸和水的混合溶液中溶解度比较大.
④分离小试管中的乙酸乙酯应使用的仪器名称是分液漏斗;分离时,乙酸乙酯应该从仪器上口倒出(填“下口放”或“上口倒出”).
⑤兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如表:
表中数据X的范围是1.57-1.76mL;实验a与实验e探究的目的是探究乙酸用量对乙酸乙酯产量的影响.
 乙醇、乙酸都是有机化工重要的基础原料.
乙醇、乙酸都是有机化工重要的基础原料.(1)空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(2)浓硫酸催化下,乙酸和乙醇生成乙酸乙酯
CH3COOH+CH3CH2OH$?_{110-120℃}^{H_{2}SO_{4}}$CH3COOH2CH3+H2O
某化学兴趣小组的同学用如图装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是大试管中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙酸.
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止倒吸.
③相关物质的部分性质:
| 乙醇 | 乙酸 | 乙酸乙酯 | |
| 沸点 | 78.0℃ | 117.9℃ | 77.5℃ |
| 水溶性 | 易溶 | 易溶 | 难溶 |
④分离小试管中的乙酸乙酯应使用的仪器名称是分液漏斗;分离时,乙酸乙酯应该从仪器上口倒出(填“下口放”或“上口倒出”).
⑤兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如表:
| 实验序号 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| a | 2 | 2 | 1.33 |
| b | 3 | 2 | 1.57 |
| c | 4 | 2 | X |
| d | 5 | 2 | 1.76 |
| e | 2 | 3 | 1.55 |