题目内容
20.2011国际化学年主题是“化学-我们的生活,我们的未来”.下列叙述正确的是( )| A. | 利用太阳能、潮汐能、煤炭发电,以获取清洁能源 | |
| B. | 反应热等于恒压体系中,反应过程产生的焓变 | |
| C. | 所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 | |
| D. | 纳米铜能在氧气中燃烧,说明了纳米铜比普通铜的还原性强 |
分析 A、太阳能、潮汐能、风力发电,均为新能源;
B、恒压时,反应热等于焓变;
C、反应吸放热与反应条件无关;
D、纳米铜能在氧气中燃烧,是因为固体表面积大的原因.
解答 解:A、太阳能、潮汐能、风力发电,均为新能源,不会对环境造成污染,为清洁能源,故A错误;
B、恒压时,反应热等于焓变,即反应热等于恒压体系中的焓变,故B正确;
C、燃烧反应均为放热反应,但反应吸放热与反应条件无关,即放热反应有的也需要加热才能发生,故C错误;
D、纳米铜的固体表面积大,故能在氧气中燃烧,故D错误.
故选B.
点评 本题考查了能源的利用、反应吸放热与反应条件的关系以及固体表面积对反应速率的影响,难度不大.注意基础的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列各组顺序的排列正确的是( )
| A. | 单质氧化性:I2>Br2>Cl2 | B. | 热稳定性:PH3>H2S>HCl | ||
| C. | 酸性强弱:HIO4>HBrO4>HClO4 | D. | 碱性强弱:KOH>NaOH>Mg(OH)2 |
8.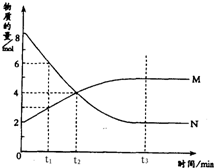 在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
 在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | t1时,N的浓度是M浓度的2倍 | |
| B. | 反应的化学方程式为N?2M | |
| C. | t2时,正逆反应速率相等,达到平衡状态 | |
| D. | t3时,正反应速率小于逆反应速率 |
15.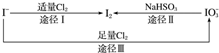 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示,下列说法中不正确的是( )
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示,下列说法中不正确的是( )
 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示,下列说法中不正确的是( )
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示,下列说法中不正确的是( )| A. | 足量Cl2能使湿润的、已变蓝的淀粉KI试纸褪色的原因可能是5Cl2+I2+6H2O═2HIO3+10HCl | |
| B. | 途径Ⅱ中若生成1 mol I2,则反应中转移的电子数为10NA | |
| C. | 用淀粉KI试纸和食醋检验加碘盐时淀粉KI试纸会变蓝 | |
| D. | 由图可知氧化性的强弱顺序为Cl2>I2>IO${\;}_{3}^{-}$ |
5.化学与生产和生活密切相关,下列说法正确的是( )
| A. | 利用化石燃料燃烧放出的热量使水分解制备氢气,是氢能开发的研究方向 | |
| B. | 石油的分馏和煤的干馏,都属于化学变化 | |
| C. | 向鸡蛋清的溶液中加入饱和(NH4)2SO4溶液,鸡蛋清因发生变性而析出 | |
| D. | 可利用二氧化碳制备全降解塑料 |
12.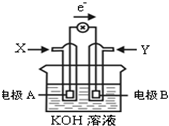 如图为某种甲醇燃料电池示意图,工作时电子流向如图所示.下列判断正确的是( )
如图为某种甲醇燃料电池示意图,工作时电子流向如图所示.下列判断正确的是( )
 如图为某种甲醇燃料电池示意图,工作时电子流向如图所示.下列判断正确的是( )
如图为某种甲醇燃料电池示意图,工作时电子流向如图所示.下列判断正确的是( )| A. | X为氧气 | |
| B. | 电极A反应式:CH3OH-6e-+H2O=CO2+6H+ | |
| C. | B电极附近溶液pH增大 | |
| D. | 电池工作时,溶液中电子由电极B流向电极A |
9.下列关于物质性质的说法不合理的是( )
| A. | 金属Mg与稀硫酸和CO2均能反应,其反应类型相同 | |
| B. | FeCl3、Na2O2、Cu2S均可由相应单质直接化合生成 | |
| C. | SO2气体通入紫色石蕊试液中,溶液先变红后褪色 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
10. 意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法不正确的是( )
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法不正确的是( )
 意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法不正确的是( )
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法不正确的是( )| A. | N4与N2互为同素异形体 | B. | N4分子中只含有共价键 | ||
| C. | 1 mol N4分子所含共价键数为6NA | D. | N4发生化学反应需要破坏离子键 |