题目内容
下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.二氧化硫被次氯酸氧化成硫酸,只能说明次氯酸具有较强氧化性,无法判断次氯酸与硫酸的酸性大小;
B.氧化铝的熔点比铝的熔点高,铝箔在酒精灯火焰上加热熔化但不滴落;
C.二氧化硅能够与碱溶液反应生成盐和水,二氧化硅属于碱性氧化物,但二氧化硅与氟化氢以外的酸不反应,不属于酸性氧化物;
D.二氧化硫与溴水发生氧化还原反应导致溴水褪色,该反应不能证明二氧化硫具有漂白性.
B.氧化铝的熔点比铝的熔点高,铝箔在酒精灯火焰上加热熔化但不滴落;
C.二氧化硅能够与碱溶液反应生成盐和水,二氧化硅属于碱性氧化物,但二氧化硅与氟化氢以外的酸不反应,不属于酸性氧化物;
D.二氧化硫与溴水发生氧化还原反应导致溴水褪色,该反应不能证明二氧化硫具有漂白性.
解答:
解:A.将SO2通入含HClO的溶液中生成H2SO4,证明次氯酸具有较强氧化性,不能证明次氯酸、硫酸的酸性大小,实际上次氯酸为弱酸,硫酸为强酸,次氯酸的酸性小于硫酸,故A错误;
B.氧化铝膜熔点高于铝,包裹在Al的外面,则铝箔在酒精灯火焰上加热熔化但不滴落,故B正确;
C.二氧化硅能够与氢氧化钠溶液反应生成盐和水,二氧化硅属于酸性氧化物,对应的酸为硅酸;而二氧化硅不与氟化氢以外的酸反应,不属于酸性氧化物,即二氧化硅不属于两性氧化物,故C错误;
D.将SO2通入溴水中,溴水褪色,溴将二氧化硫氧化成硫酸,从而导致溴水褪色,溴水褪色原因不是因为二氧化硫具有漂白性,故D错误;
故选B.
B.氧化铝膜熔点高于铝,包裹在Al的外面,则铝箔在酒精灯火焰上加热熔化但不滴落,故B正确;
C.二氧化硅能够与氢氧化钠溶液反应生成盐和水,二氧化硅属于酸性氧化物,对应的酸为硅酸;而二氧化硅不与氟化氢以外的酸反应,不属于酸性氧化物,即二氧化硅不属于两性氧化物,故C错误;
D.将SO2通入溴水中,溴水褪色,溴将二氧化硫氧化成硫酸,从而导致溴水褪色,溴水褪色原因不是因为二氧化硫具有漂白性,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及氧化还原反应与金属性和酸性比较、二氧化硅的性质、次氯酸的性质等,题目难度中等,把握化学反应原理及物质性质为解答的关键,注意对常见化学实验方案的评价方法.

练习册系列答案
相关题目
常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是( )
| A、pH>7,且 c(OH-)>c(Na+)>c(H+)>c(CH3COO-) |
| B、pH>7,且 c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C、pH=7,且c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
| D、pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
由1-丙醇制取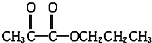 ,最简便的流程需要下列反应的顺序应是( )
,最简便的流程需要下列反应的顺序应是( )
a.氧化 b.还原 c.取代 d.加成 e.消去 f.中和 g.加聚 h.酯化.
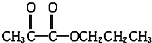 ,最简便的流程需要下列反应的顺序应是( )
,最简便的流程需要下列反应的顺序应是( )a.氧化 b.还原 c.取代 d.加成 e.消去 f.中和 g.加聚 h.酯化.
| A、e、d、c、a、h |
| B、b、d、f、g、h |
| C、a、e、d、c、h |
| D、b、a、e、c、f |
下列各组物质,不用任何化学试剂即可鉴别的是( )
| A、氯水、NaBr溶液、盐酸 |
| B、NaCl溶液、NaBr溶液、KI溶液 |
| C、氯化氢、溴化氢、碘化氢 |
| D、盐酸、NaCl溶液、AgNO3溶液、Na2CO3溶液 |
下列说法中正确的是( )
| A、凡能发生银镜反应的有机物一定是醛 |
| B、酸和醇发生的反应一定是酯化反应 |
| C、乙醇易溶于水是因为分子间形成了一种叫氢键的化学键 |
| D、在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成水和酯 |
下列装置或操作能达到实验目的是( )
A、 除去乙醇中的乙酸 |
B、 形成原电池 |
C、 制取乙酸乙酯 |
D、 甲烷的取代反应 |
有如下几种物质,①蔗糖②麦芽糖③甲酸甲酯④淀粉,水解前后都能发生银镜反应的( )
| A、①②③ | B、①③ |
| C、②③ | D、①②③④ |