题目内容
常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是( )
| A、pH>7,且 c(OH-)>c(Na+)>c(H+)>c(CH3COO-) |
| B、pH>7,且 c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C、pH=7,且c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
| D、pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.pH>7,溶液为碱性,由于醋酸与氢氧化钠反应,则不可能出现c(OH-)>c(Na+);
B.溶液中一定满足电荷守恒,根据电荷守恒判断;
C.pH=7,溶液为中性,根据电荷守恒判断各离子浓度关系;
D.pH<7,当醋酸远远过量,氢氧化钠很少时可以出现c(CH3COO-)>c(H+)>c(Na+)>c(OH-).
B.溶液中一定满足电荷守恒,根据电荷守恒判断;
C.pH=7,溶液为中性,根据电荷守恒判断各离子浓度关系;
D.pH<7,当醋酸远远过量,氢氧化钠很少时可以出现c(CH3COO-)>c(H+)>c(Na+)>c(OH-).
解答:
解:A.pH>7,则c(OH-)>c(H+),因为氢离子和氢氧根离子反应生成水,所以不可能出现c(OH-)>c(Na+)、c(H+)>c(CH3COO-),故A错误;
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),故B正确;
C.pH=7,溶液显示中性,则c(H+)=c(OH-),根据电荷守恒得c(CH3COO-)=c(Na+),溶液中离子浓度大小为:c(CH3COO-)=c(Na+)>c(H+)=c(OH-),故C正确;
D.pH<7,则c(OH-)<c(H+),如果NaOH的量很小,则存在c(CH3COO-)>c(H+)>c(Na+)>c(OH-),故D正确;
故选A.
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),故B正确;
C.pH=7,溶液显示中性,则c(H+)=c(OH-),根据电荷守恒得c(CH3COO-)=c(Na+),溶液中离子浓度大小为:c(CH3COO-)=c(Na+)>c(H+)=c(OH-),故C正确;
D.pH<7,则c(OH-)<c(H+),如果NaOH的量很小,则存在c(CH3COO-)>c(H+)>c(Na+)>c(OH-),故D正确;
故选A.
点评:本题考查了酸碱混合溶液定性判断、离子浓度大小比较,题目难度中等,根据溶液中的溶质及溶液酸碱性再结合守恒思想分析解答,根据溶液酸碱性确定溶液中的溶质为解答关键.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、Ba(OH)2溶液中滴入足量的NaHCO3溶液:Ba2++OH-+HCO3-═BaCO3↓+H2O |
| B、Ba(OH)2溶液中滴入CuSO4溶液:2OH-+Cu2+═Cu(OH)2↓ |
| C、盐酸和澄清的石灰水混合:H++OH-═H2O |
| D、Cu与浓硫酸反应:Cu+4H++SO42-═Cu2++SO2↑+2H2O |
试管里有一黑色粉末状固体,加热后有红色固体生成,同时还生成一种无色无味且能使澄清石灰水变浑浊的气体.此固体物质可能是( )
| A、氧化铜和木炭粉的混合物 |
| B、氧化铁和木炭粉的混合物 |
| C、木炭粉 |
| D、氧化铜和二氧化锰的混合物 |
不能用化学平衡移动原理来说明的事实是( )
| A、合成氨在高压下进行是有利的 |
| B、温度过高对合成氨不利 |
| C、使用催化剂能使合成氨速率加快 |
| D、及时分离从合成塔中出来的混合气,有利于合成氨 |
要除去混在氮气中的二氧化碳和一氧化碳得到纯净、干燥的氮气,正确方法是( )
| A、先通过石灰水,在通过灼热的氧化铜 |
| B、先通过常温下的氧化铜,再通过氢氧化钠 |
| C、先通过灼热的氧化铜,再通过氢氧化钠溶液,最后通过浓硫酸 |
| D、先通过灼热的铜,再通过石灰水 |
已知铅+2价稳定,+4价铅有很强的氧化性,今有6种下列物质:H2O、PbO2、Pb(NO3)2、HMnO4、HNO3和Mn(NO3)2组成一个化学方程式.下列有关说法正确的是( )
| A、反应物中发生氧化反应的物质PbO2 |
| B、被还原的元素是Mn(NO3)2中Mn |
| C、反应中1mol氧化剂得到5mol电子 |
| D、请将反应物配平后的PbO2与Mn(NO3)2系数之比5:2 |
下列药品可用带玻璃塞的试剂瓶储存的是( )
| A、稀盐酸 |
| B、氢氟酸 |
| C、NaOH溶液 |
| D、Na2SiO3溶液 |
某同学设计如图所示装置,探究氯碱工业原理,下列说法正确的是( )
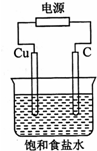

| A、石墨电极与直流电源负极相连 |
| B、用湿润KI淀粉试剂在铜电极附近检验气体,试纸变蓝色 |
| C、氢氧化钠在石墨电极附近产生,Na+向石墨电极迁移 |
| D、铜电极的反应式为:2H++2e-═H2↑ |