题目内容
某研究小组想研究碳与浓硝酸的反应.其实验过程如下.
(1)热的浓硝酸与红热的木炭接触会发生多个化学反应.
①碳与浓硝酸的反应,说明浓硝酸具有 性.
②反应产生的热量会使少量浓硝酸受热分解,产生红棕色气体、一种无色无味的单质气体X和水,气体X的化学式是 .
(2)实验现象中液面上木炭迅速燃烧,发出光亮.同学甲认为可能是木炭与气体X反应产生的现象;同学乙猜测NO2可能具有助燃性,木炭能在NO2中燃烧.他们设计了以下实验.
Ⅰ.制取NO2气体.
①在虚线框内画出用铜与浓硝酸制取和收集NO2的装置简图(夹持仪器略).
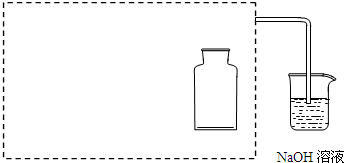
②NaOH溶液的作用是吸收多余的NO2,该反应生成两种物质的量相等的正盐,写出反应的化学方程式 .
Ⅱ.探究实验.
实验操作:在空气中引燃木炭,使其燃烧并带有火焰,将带火焰的木炭伸入盛有NO2气体的集气瓶中.
实验现象:木炭在NO2气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色.
①根据实验现象写出碳与NO2气体反应的化学方程式 .
②试分析是否需要增加带火焰的木炭与纯净的X气体反应的实验 .
③通过实验探究,你认为甲、乙同学的预测是否合理,请简述理由 .
| 操作 | 现象 |
| a.用干燥洁净的烧杯取约10mL浓硝酸,加热. | / |
| b.把小块烧红的木炭迅速伸入热的浓硝酸中. | 红热的木炭与热的浓硝酸接触发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧,发出光亮. |
①碳与浓硝酸的反应,说明浓硝酸具有
②反应产生的热量会使少量浓硝酸受热分解,产生红棕色气体、一种无色无味的单质气体X和水,气体X的化学式是
(2)实验现象中液面上木炭迅速燃烧,发出光亮.同学甲认为可能是木炭与气体X反应产生的现象;同学乙猜测NO2可能具有助燃性,木炭能在NO2中燃烧.他们设计了以下实验.
Ⅰ.制取NO2气体.
①在虚线框内画出用铜与浓硝酸制取和收集NO2的装置简图(夹持仪器略).

②NaOH溶液的作用是吸收多余的NO2,该反应生成两种物质的量相等的正盐,写出反应的化学方程式
Ⅱ.探究实验.
实验操作:在空气中引燃木炭,使其燃烧并带有火焰,将带火焰的木炭伸入盛有NO2气体的集气瓶中.
实验现象:木炭在NO2气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色.
①根据实验现象写出碳与NO2气体反应的化学方程式
②试分析是否需要增加带火焰的木炭与纯净的X气体反应的实验
③通过实验探究,你认为甲、乙同学的预测是否合理,请简述理由
考点:性质实验方案的设计
专题:实验设计题
分析:(1)①碳与浓硝酸的反应中,碳被氧化为二氧化碳,浓硝酸中的氮被还原为二氧化氮,据此推断;
②浓硝酸受热分解,产生红棕色气体应为二氧化氮,根据氧化还原反应的原理可知,氮的化合价降低,则氧的化合价升高,结合产生一种无色无味的单质气体可知该气体为氧气,据此答题;
(2)Ⅰ①铜与浓硝酸反应为固体和液体的反应,不需要加热,生成的NO2的能和水反应,密度比空气大,所以要用向上排空气法收集,据此可画出装置图;
②NaOH溶液与NO2反应生成两种物质的量相等的正盐为硝酸钠和亚硝酸钠,根据氧化还原反应的原理结合元素守恒可写出化学方程式;
Ⅱ①木炭在NO2气体中燃,结合元素守恒分析,产生的气体能使澄清石灰水变浑浊则为二氧化碳,另一种无色气体且遇空气不变色,则为氮气;据此写出化学方程式;
②木炭在NO2气体中持续燃烧,火焰迅速变亮,本身就能说明碳与NO2气体能发生反应,另外在反应过程中体系中氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验,据此答题;
③液面上木炭迅速燃烧,发出光亮,结合后面的对比实验可以看出,碳主要是和NO2的燃烧反应,也会发生与氧气的燃烧反应,因为两种气体在液面上方均存在,据此答题.
②浓硝酸受热分解,产生红棕色气体应为二氧化氮,根据氧化还原反应的原理可知,氮的化合价降低,则氧的化合价升高,结合产生一种无色无味的单质气体可知该气体为氧气,据此答题;
(2)Ⅰ①铜与浓硝酸反应为固体和液体的反应,不需要加热,生成的NO2的能和水反应,密度比空气大,所以要用向上排空气法收集,据此可画出装置图;
②NaOH溶液与NO2反应生成两种物质的量相等的正盐为硝酸钠和亚硝酸钠,根据氧化还原反应的原理结合元素守恒可写出化学方程式;
Ⅱ①木炭在NO2气体中燃,结合元素守恒分析,产生的气体能使澄清石灰水变浑浊则为二氧化碳,另一种无色气体且遇空气不变色,则为氮气;据此写出化学方程式;
②木炭在NO2气体中持续燃烧,火焰迅速变亮,本身就能说明碳与NO2气体能发生反应,另外在反应过程中体系中氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验,据此答题;
③液面上木炭迅速燃烧,发出光亮,结合后面的对比实验可以看出,碳主要是和NO2的燃烧反应,也会发生与氧气的燃烧反应,因为两种气体在液面上方均存在,据此答题.
解答:
解:(1)①碳与浓硝酸的反应中,碳被氧化为二氧化碳,浓硝酸中的氮被还原为二氧化氮,说明浓硝酸具有强氧化性,故答案为:强氧化性;
②浓硝酸受热分解,产生红棕色气体应为二氧化氮,根据氧化还原反应的原理可知,氮的化合价降低,则氧的化合价升高,结合产生一种无色无味的单质气体可知该气体为氧气,故答案为:O2;
(2)Ⅰ①铜与浓硝酸反应为固体和液体的反应,不需要加热,生成的NO2的能和水反应,密度比空气大,所以要用向上排空气法收集,据此可画出装置图为 ,
,
故答案为: ;
;
②NaOH溶液与NO2反应生成两种物质的量相等的正盐为硝酸钠和亚硝酸钠,根据氧化还原反应的原理结合元素守恒可写出化学方程式为:2NO2+2NaOH═NaNO2+NaNO3+H2O,故答案为:2NO2+2NaOH═NaNO2+NaNO3+H2O;
Ⅱ①木炭在NO2气体中燃,结合元素守恒分析,产生的气体能使澄清石灰水变浑浊则为二氧化碳,另一种无色气体且遇空气不变色,则为氮气;据此写出化学方程式为:2NO2+2C
N2+2CO2,
故答案为:2NO2+2C
N2+2CO2;
②因为在反应过程中体系中有NO2气体存在,所以氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验,
故答案为:当木炭燃烧时,体系中氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验;
③液面上木炭迅速燃烧,发出光亮,结合后面的对比实验可以看出,碳主要是和NO2的燃烧反应,也会发生与氧气的燃烧反应,因为两种气体在液面上方均存在,
故答案为:主要是和NO2的燃烧反应,也会发生与氧气的燃烧反应,因为两种气体均存在.
②浓硝酸受热分解,产生红棕色气体应为二氧化氮,根据氧化还原反应的原理可知,氮的化合价降低,则氧的化合价升高,结合产生一种无色无味的单质气体可知该气体为氧气,故答案为:O2;
(2)Ⅰ①铜与浓硝酸反应为固体和液体的反应,不需要加热,生成的NO2的能和水反应,密度比空气大,所以要用向上排空气法收集,据此可画出装置图为
 ,
,故答案为:
 ;
;②NaOH溶液与NO2反应生成两种物质的量相等的正盐为硝酸钠和亚硝酸钠,根据氧化还原反应的原理结合元素守恒可写出化学方程式为:2NO2+2NaOH═NaNO2+NaNO3+H2O,故答案为:2NO2+2NaOH═NaNO2+NaNO3+H2O;
Ⅱ①木炭在NO2气体中燃,结合元素守恒分析,产生的气体能使澄清石灰水变浑浊则为二氧化碳,另一种无色气体且遇空气不变色,则为氮气;据此写出化学方程式为:2NO2+2C
| ||
故答案为:2NO2+2C
| ||
②因为在反应过程中体系中有NO2气体存在,所以氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验,
故答案为:当木炭燃烧时,体系中氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验;
③液面上木炭迅速燃烧,发出光亮,结合后面的对比实验可以看出,碳主要是和NO2的燃烧反应,也会发生与氧气的燃烧反应,因为两种气体在液面上方均存在,
故答案为:主要是和NO2的燃烧反应,也会发生与氧气的燃烧反应,因为两种气体均存在.
点评:本题主要考查学生分析实验和书写化学方程式的能力,尤其是对实验原理的分析要求较高,要求学生有较高的逻辑推理能力和扎实的实验基本功及作图能力,难度较大.

练习册系列答案
相关题目
下面的化学实验各操作正确的一组是:( )
①蒸发操作,待蒸发皿中的水基本蒸干时,就可停止加热;蒸馏时冷却水从冷凝管下端进入,上端出来.
②向天平托盘中加少量固体时应用右手拿药匙,左手轻轻拍打右手的手腕,让少量药品掉落托盘上;
③过滤时,使漏斗下端管口垂直的一面紧靠烧杯内壁,洗涤沉淀时不能用玻璃棒搅拌;
④玻璃仪器洗后,如果内壁的水附着均匀,既不聚成水滴也不成股流下,才算洗干净.
①蒸发操作,待蒸发皿中的水基本蒸干时,就可停止加热;蒸馏时冷却水从冷凝管下端进入,上端出来.
②向天平托盘中加少量固体时应用右手拿药匙,左手轻轻拍打右手的手腕,让少量药品掉落托盘上;
③过滤时,使漏斗下端管口垂直的一面紧靠烧杯内壁,洗涤沉淀时不能用玻璃棒搅拌;
④玻璃仪器洗后,如果内壁的水附着均匀,既不聚成水滴也不成股流下,才算洗干净.
| A、①②④ | B、①②③ |
| C、①③④ | D、②③④ |
下列有关焓(H)判据和熵(S)判据的叙述正确的是( )
| A、△H>0的反应使体系能量升高,不能自发进行 |
| B、△H<0的反应使体系能量降低,无需加热便能自发进行 |
| C、在与外界隔离的体系中,自发过程将导致熵增大 |
| D、熵增原理说明△S<0过程在任何条件下都不能自发进行 |


 表示的分子式
表示的分子式