题目内容
16.硫酸是中学化学实验室的常见药品,其性质有①酸性 ②吸水性 ③脱水性 ④强氧化性,请将序号填在相应的横线上:(1)锌和稀H2SO4制H2①;
(2)浓硫酸作干燥剂②;
(3)浓硫酸与蔗糖的炭化实验(黑面包实验)②③④;
(4)浓硫酸与铜的反应①④;
(5)浓硫酸使湿润的蓝色石蕊试纸先变红,后来又变黑①③.
分析 (1)稀硫酸具有酸性和金属反应生成氢气;
(2)浓硫酸具有吸水性,可以干燥气体;
(3)浓硫酸具有脱水性,蔗糖中氢和氧原子按照2:1脱去发生炭化现象,炭与浓硫酸发生氧化还原反应生成二氧化碳和水、二氧化硫;
(4)浓硫酸和铜在加热条件下反应生成硫酸铜和二氧化硫和水,依据硫元素化合价变化判断浓硫酸的性质;
(5)浓硫酸使润湿蓝色石蕊试纸先变红后又变黑,体现浓硫酸的酸性和脱水性.
解答 解:(1)锌和稀H2SO4制H2利用的是稀硫酸的酸性,
故答案为:①;
(2)浓硫酸具有吸水性,能吸收气体中的水蒸气可用作气体干燥剂,
故答案为:②;
(3)浓硫酸与蔗糖的炭化实验体现了浓硫酸具有脱水性,蔗糖中氢和氧原子按照2:1脱去发生炭化现象,
故答案为:②③④;
(4)浓硫酸和铜在加热条件下反应,生成二氧化硫和硫酸铜、水,硫元素化合价部分降低,部分不变,所以既表现了浓硫酸的强氧化性又表现了酸性,故答案为:①④;
(5)浓硫酸具有酸性,所以能使湿润的蓝色石蕊试纸变红色,浓硫酸能将纸张中H、O元素以2:1水的形式脱去而体现脱水性,
故答案为:①③.
点评 本题考查了稀硫酸、浓硫酸的性质,稀硫酸和浓硫酸具有酸性,浓硫酸还有特殊性吸水性、脱水性和强氧化性,注意吸水性和脱水性的区别,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列说法错误的是( )
| A. | 纯铁比生铁更耐腐蚀 | |
| B. | 明矾水解形成胶体能吸附悬浮物,可用于净水 | |
| C. | 碳酸钠溶液呈碱性是因为其在水中电离出OH- | |
| D. | 工业废水中的Cu2+和Hg2+可用Na2S或H2S除去 |
7. 在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.实验中其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).根据图示判断下列说法不正确的是( )
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.实验中其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).根据图示判断下列说法不正确的是( )
 在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.实验中其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).根据图示判断下列说法不正确的是( )
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.实验中其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).根据图示判断下列说法不正确的是( )| A. | 实验进行时试管 A 中应加入的试剂是普通铁粉 | |
| B. | 烧瓶 B 的作用是防止倒吸,烧瓶 C 的作用是产生水蒸气 | |
| C. | 试管 D 中收集得到的是 H2 | |
| D. | 3 mol 单质 Fe 全部转变为 Fe3O4,失去 8 mol 电子 |
4.下列叙述正确的是( )
| A. | 强电解质都是离子化合物,弱电解质都是共价化合物 | |
| B. | 强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子 | |
| C. | 向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体 | |
| D. | 向Na2CO3饱和溶液中,通入过量的CO2后,加热蒸干得NaHCO3晶体 |
11.有Fe和Fe2O3的混合物27.2g溶于100ml的稀硫酸中,恰好完全反应,放出H22.24L(标况下),向反应后的溶液中滴入无色KSCN溶液,未见血红色.混合物中单质Fe的质量为( )
| A. | 5.6g | B. | 8.4g | C. | 11.2g | D. | 16.8g |
1.设NA为阿伏加德罗常数的值,下列说法一定正确的是( )
| A. | 0.1mol FeCl3能形成的胶体粒子数为0.1NA | |
| B. | 常温下1L pH=12氨水中含有OH-数目为0.01NA | |
| C. | 0.1mol02完全反应时,转移的电子数为0.4NA | |
| D. | 12克碳单质中所含的共价键数为2NA |
8.人工光合作用能够借助太阳能,用CO2和H2O制备CH4的原理如图所示.下列有关说法不正确的是( )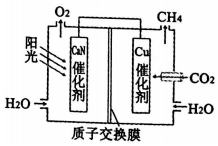

| A. | 该装置是原电池 | |
| B. | GaN催化剂表面发生氧化反应,溶液酸性增强 | |
| C. | 电子从GaN催化剂经导线转移到Cu催化剂 | |
| D. | Cu催化剂表面的反应是CO2+8H++8e-=CH4+2H2O |
5.某温度下,将2molSO2和1molO2置于10L密闭容器中发生反应:2SO2(g)+O2(g)$→_{△}^{催化剂}$2SO3(g);△H<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( )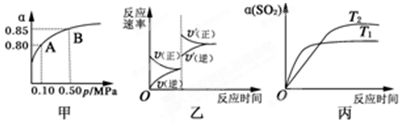

| A. | 由图甲推断,B点SO2的平衡浓度为0.3 mol•L-1 | |
| B. | 由图甲推断,A点对应温度下该反应的平衡常数为800(L•mol-1) | |
| C. | 达平衡后,若增大容器容积,则反应速率变化图象可以用图乙表示 | |
| D. | 压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
10.在相同压强下,经过相同反应时间测得如下实验数据:
【备注】甲醇选择性:转化的CO2中生成甲醇的百分比.
(1)测得实验数据时,反应不是(填“是”或“不是”)处于平衡状态.
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有CD
A.使用催化剂A B.使用催化剂B C.降低反应温度 D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明:在相同温度下,因为催化剂A和B对反应Ⅰ的催化能力不同,所以在该时刻不同的催化剂对CO2转化成CH3OH的选择性有显著的影响.
| 实验编号 | T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 1 | 543 | 催化剂A | 12.3 | 42.3 |
| 2 | 543 | 催化剂B | 10.9 | 72.7 |
| 3 | 553 | 催化剂A | 15.3 | 39.1 |
| 4 | 553 | 催化剂B | 12.0 | 71.6 |
(1)测得实验数据时,反应不是(填“是”或“不是”)处于平衡状态.
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有CD
A.使用催化剂A B.使用催化剂B C.降低反应温度 D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明:在相同温度下,因为催化剂A和B对反应Ⅰ的催化能力不同,所以在该时刻不同的催化剂对CO2转化成CH3OH的选择性有显著的影响.