题目内容
7.下列说法中正确的是( )| A. | 1molS的质量是32g/mol | B. | 27g铝的物质的量为1 | ||
| C. | CO的摩尔质量为28g/mol | D. | 2H2O的摩尔质量为18g/mol |
分析 A.质量的单位为g;
B.物质的量的单位为mol;
C.摩尔质量的单位为g/mol,在数值上等于相对分子质量;
D.2H2O的相对分子质量为20.
解答 解:A.质量的单位为g,则1molS的质量是32g,故A错误;
B.物质的量的单位为mol,所以27g铝的物质的量为1mol,故B错误;
C.摩尔质量的单位为g/mol,在数值上等于相对分子质量,则CO的摩尔质量为28g/mol,故C正确;
D.2H2O的相对分子质量为20,2H2O的摩尔质量为20g/mol,故D错误.
故选C.
点评 本题考查了物质的量、摩尔质量的概念和单位,题目难度不大,注意把握有关概念,明确摩尔质量的单位为g/mol及在数值上等于相对分子质量是解题的关键.

练习册系列答案
相关题目
17.已知Br2、Fe2(SO4)3、CaC2等物质均能与水发生反应,生成两种物质.下表中所列四种物质都易与水反应.
(1)在表中空格处填写各物质分别与水反应的产物中,属于氧化物对应水化物的化学式
(2)写出这四种物质与水反应的产物中,分子构型为正四面体的结构式
(3)由氨水和次氯酸盐溶液在弱碱性介质中反应可生成氯胺H2NCl,分子结构类似于NH3,H2NCl分子的空间构型为三角锥型,电子式为$\underset{\stackrel{\;}{H:}}{\;}\underset{\stackrel{\underset{H}{••}}{N}}{••}\underset{\stackrel{\;}{:}}{\;}\underset{\stackrel{••}{Cl}}{••}\underset{\stackrel{\;}{:}}{\;}$.
(1)在表中空格处填写各物质分别与水反应的产物中,属于氧化物对应水化物的化学式
| Li3N | NaNH2 | SiBr4 | Mg2Si |

(3)由氨水和次氯酸盐溶液在弱碱性介质中反应可生成氯胺H2NCl,分子结构类似于NH3,H2NCl分子的空间构型为三角锥型,电子式为$\underset{\stackrel{\;}{H:}}{\;}\underset{\stackrel{\underset{H}{••}}{N}}{••}\underset{\stackrel{\;}{:}}{\;}\underset{\stackrel{••}{Cl}}{••}\underset{\stackrel{\;}{:}}{\;}$.
15.某烃不与溴水反应,能使酸性高锰酸钾溶液褪色,在Fe存在下与Cl2反应,能生成两种一氯代物,该烃是( )
| A. | CH≡C-CH3 | B. | 对二甲苯 | ||
| C. | 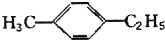 | D. | 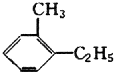 |
2.下列说法正确的是( )
| A. | 纯净物是指由同种元素组成的物质 | B. | 由同种元素组成的纯净物叫单质 | ||
| C. | 由不同种分子组成的物质叫化合物 | D. | 一种元素只能组成一种单质 |
12.填写下表中的空格:
| 微粒符号 | 质子数 | 中子数 | 电子数 | 质量数 |
| (1)${\;}_{19}^{40}$K | 19 | 40 | ||
| (2) | 16 | 18 | 32 |
17.已知Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0,下列叙述不正确的是( )
| A. | 该反应中旧键断裂吸收的总能量大于新键形成放出的总能量 | |
| B. | 反应物的总能量高于生成物的总能量 | |
| C. | 该反应为放热反应 | |
| D. | 该反应的化学能可以转化为电能 |
 ”标志的是c(选填字母).
”标志的是c(选填字母).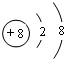 .
.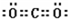 .
.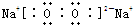 ,其中含有的化学键有离子键、共价键.用电子式表示B、D的单质在常温下反应生成的化合物的形成过程:
,其中含有的化学键有离子键、共价键.用电子式表示B、D的单质在常温下反应生成的化合物的形成过程: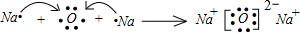 .
.