题目内容
12.填写下表中的空格:| 微粒符号 | 质子数 | 中子数 | 电子数 | 质量数 |
| (1)${\;}_{19}^{40}$K | 19 | 40 | ||
| (2) | 16 | 18 | 32 |
分析 原子中:质量数=质子数+中子数,质子数=电子数,结合原子的组成分析.
解答 解:(1)${\;}_{19}^{40}$K中质子数=19,质量数=40,则中子数=40-19=21,电子数=质子数=19
(2)质子数=32-16=16,电子数=18,电子数比质子数多2,属于阴离子,所以微粒为1632S2-;
故答案为:
| 微粒符号 | 质子数 | 中子数 | 电子数 | 质量数 |
| (1)${\;}_{19}^{40}$K | 19 | 21 | 19 | 40 |
| (2)1632S2- | 16 | 16 | 18 | 32 |
点评 本题考查了微粒的构成,题目难度不大,注意原子中质量数=质子数+中子数,质子数=电子数,侧重于基础知识的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列物质是最常见的温室气体( )
| A. | O2 | B. | H2 | C. | CO2 | D. | Cl2 |
20.下列实验操作正确的是( )
| A. | 将氢氧化钠固体放在滤纸上称量 | |
| B. | 用强光照射鉴别淀粉胶体与碳酸钠溶液 | |
| C. | 用10mL量筒量取8.58mL蒸馏水 | |
| D. | 蒸馏时,应将温度计的水银球插入液面以下 |
7.下列说法中正确的是( )
| A. | 1molS的质量是32g/mol | B. | 27g铝的物质的量为1 | ||
| C. | CO的摩尔质量为28g/mol | D. | 2H2O的摩尔质量为18g/mol |
17.800℃时,a、b、c三种气态物的浓度随时间变化的情况如图,由图分析不能得出的结论是( )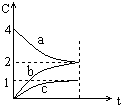

| A. | a是反应物 | B. | 正反应是一个体积扩大的反应 | ||
| C. | 若升高温度,a的转化率增大 | D. | 若增大压强,a的转化率减小 |
1.下列反应过程中,最终溶液保持原来颜色的是( )
| A. | 向滴有酚酞的NaOH溶液中通入过量的CO2气体 | |
| B. | 向酸性KMnO4溶液中加入足量的H2O2 | |
| C. | 向含有KSCN的FeC13溶液中加入足量的Cu粉 | |
| D. | 向品红溶液中通入足量的等体积混合的Cl2与SO2气体 |
2.下列说法正确的是( )
| A. | 在Na2CO3、NaHCO3两溶液中,离子种类不相同 | |
| B. | 在NaHCO3溶液中有c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) | |
| C. | 在Na2CO3溶液中有c(OH-)=c(H+)+c(HCO3-)+2 c(H2CO3) | |
| D. | 在Na2CO3溶液中有2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
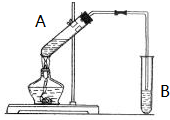 实验室用如图所示的装置制取乙酸乙酯.
实验室用如图所示的装置制取乙酸乙酯. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.